
【题目】根据《化学反应原理》中相关知识,按要求作答。
氯的单质、化合物与人类生产、生活和科研密切相关。
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式: H2(g)+Cl2(g)=2HCl(g)△H = -184.6 kJ . mol-1,判断该反应属于_____(填“吸热”或“放热")反应。
(2)盐酸是一种强酸,补充完整电离方程式:HCl=___+Cl- 。室温下,将大小相等的镁条和铁片投入同浓度的稀盐酸中,产生氢气的速率较大的是________。
(3)84消毒液在防控新冠肺炎疫情中被大量使用,它是利用氯气与氢氧化钠溶液反应制成的.反应方程式为Cl2+2NaOH=NaCl+NaClO+H2O。
①该反应____(填“是”或“不是”)氧化还原反应。
②室温下,84消毒液呈碱性,其pH___7 (填“>”或“<”)。
③84消毒液的有效成分NaClO,水解的离子方程式:ClO-+H2O=HClO+OH-,生成物中__具有很强的氧化性,可以使病毒和细菌失去生理活性;水解是吸热反应,升高温度平衡向_____(填“正反应”或“逆反应”)方向移动。
(4)电解熔融氯化钠可制取金属钠和氯气,装置如图所示(电极不参与反应):
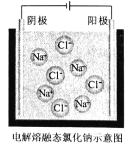
通电时,Na+向______(填“阳极”或“阴极")移动,写出生成金属钠的电极反应式:______。
【答案】放热 H+ 镁条 是 > HClO 正反应 阴极 Na++e-=Na
【解析】
根据焓变△H<0,反应放热进行判断;根据强酸的电离方程式书写盐酸的电离方程式,根据镁和铁的活泼性进行判断;根据化合价的变化判断是否是氧化还原反应原理;根据盐类的水解原理回答;根据电解氯化钠的原理进行回答;
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式:H2(g)+Cl2(g)=2HCl(g)△H = -184.6 kJ . mol-1,△H<0,反应物具有的总能量高于生成物的总能量,该反应属于放热反应;
(2)盐酸是一种强酸,电离方程式:HCl=H++Cl-,室温下,将大小相等的镁条和铁片投入同浓度的稀盐酸中,产生氢气的速率较大的是镁,镁比铁活泼,反应速率更快;
(3)84消毒液在防控新冠肺炎疫情中被大量使用,它是利用氯气与氢氧化钠溶液反应制成的.反应方程式为Cl2+2NaOH=NaCl+NaClO+H2O;
①氯气的化合价从0价升高到+1价,降低到-1价,有化合价的变化,是氧化还原反应;
②室温下,84消毒液呈碱性,主要成分为次氯酸钠,属于强碱弱酸盐,显碱性,其pH>7;
③84消毒液的有效成分NaClO,水解的离子方程式:ClO-+H2O![]() HClO+OH-,生成物中HClO具有很强的氧化性,可以使病毒和细菌失去生理活性;水解是吸热反应,升高温度平衡向吸热的方向移动,反应向正反应方向移动;
HClO+OH-,生成物中HClO具有很强的氧化性,可以使病毒和细菌失去生理活性;水解是吸热反应,升高温度平衡向吸热的方向移动,反应向正反应方向移动;
(4)电解熔融氯化钠可制取金属钠和氯气,通电时,阳离子移向阴极,阴离子移向阳极,Na+向阴极移动,在阴极上得到电子,生成金属钠,电极反应式为:Na++e-=Na。


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】如图所示,电化学原理与微生物工艺相组合的电解脱硝法,可除去引起水华的NO3-原理是将NO3-还原为N2。下列说法正确的是( )
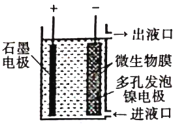
A. 若加人的是![]() 溶液,则导出的溶液呈碱性
溶液,则导出的溶液呈碱性
B. 镍电极上的电极反应式为:![]()
C. 电子由石墨电极流出,经溶液流向镍电极
D. 若阳极生成![]() 气体,理论上可除去
气体,理论上可除去![]() mol
mol![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员研究了在Cu-ZnO-ZrO2催化剂上CO2加氢制甲醇过程中水的作用机理,其主反应历程如图所示(H2→*H+*H)。下列说法错误的是
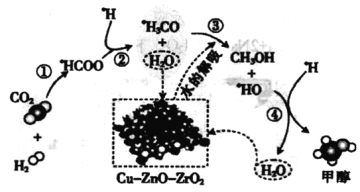
A.催化剂不能提高二氧化碳加氢制甲醇的过程中原子利用率
B.该反应过程中,涉及了极性共价键的断裂和生成
C.第③步的反应式为*H3CO+H2O→CH3O*H+HO
D.向该反应体系中加入少量的水能增加甲醇的产率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一氧化氮-空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的SO2、NO转化为(NH4)2SO4的原理和粗铜的精炼原理。
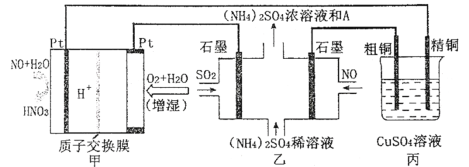
(1)燃料电池放电过程中负极的电极反应式____。
(2)乙装置中物质A是____(填化学式),理由是___;电解过程中阳极附近pH___(填“增大”“减小”或“不变”),阴极的电极反应式是____。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将__(填“增大”、“减小”或“不变”)。
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质的量共有____mol;丙装置中阴极析出铜的质量为___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W原子序数依次增加,X原子的半径小于Y原子,Y是地壳中含量最高的元素,Z原子的最外层只有1个电子,Y、W同主族。下列说法正确的是( )
A.原子半径:![]() B.Y与Z形成的化合物中只含离子键
B.Y与Z形成的化合物中只含离子键
C.W元素形成的最高价氧化物的水化物是强酸D.X与Z形成的化合物中X为![]() 价
价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化亚铜是一种白色粉末,不溶于冷水,在热水中或见光都会分解,在空气中会慢慢被氧化。实验室制备![]() 的步骤如下:
的步骤如下:
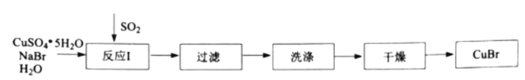
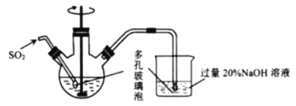
(1)反应Ⅰ在如图所示实验装置的三颈烧瓶中进行,实验所用蒸馏水需经煮沸,目的是除去水中的_________(写化学式)。
(2)反应Ⅰ中:三颈烧瓶中反应生成![]() 的离子方程式为________;烧杯中发生反应的化学方程式为________。
的离子方程式为________;烧杯中发生反应的化学方程式为________。
(3)过滤步骤中,需要在避光的条件下进行,原因是________。
(4)洗涤步骤中,依次用溶有少量![]() 的水、溶有少量
的水、溶有少量![]() 的乙醇、纯乙醚洗涤。洗涤剂需“溶有
的乙醇、纯乙醚洗涤。洗涤剂需“溶有![]() ”的原因是________。
”的原因是________。
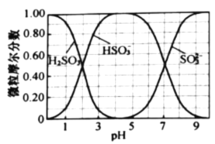
(5)欲利用上述装置烧杯中的吸收液制取较纯净的无水![]() 晶体。
晶体。
(水溶液中![]() 、
、![]() 、
、![]() 随
随![]() 的分布,
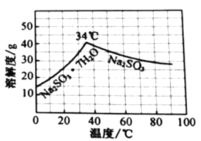
的分布,![]() 的溶解度曲线如题图所示)。
的溶解度曲线如题图所示)。
请补充完整实验方案[须用到![]() (贮存在钢瓶中)、
(贮存在钢瓶中)、![]() 计]:
计]:
①________;
②加入少量维生素C溶液(抗氧剂),加热浓缩溶液至有大量晶体析出;
③________;
④用无水乙醇洗涤2-3次;
⑤放真空干燥箱中干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用核磁共振仪对分子式为C3H8O的有机物进行分析,核磁共振氢谱有三个峰,峰面积之比是1:1:6,则该化合物的结构简式为
A.CH3-O-CH2-CH3B.![]()
C.CH3CH2CH2OHD.C3H7OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、磷及其化合物在生产、生活中有重要的用途。回答下列问题:
Ⅰ.(1)氮的固定是几百年来科学家一直研究的课题。
下表列举了不同温度下大气固氮和工业固氮的部分K值。
反应 | 大气固氮 N2(g)+O2(g) | 工业固氮 N2(g)+3H2(g) | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
K | 3.8×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
①分析数据可知:大气固氮反应属于_____(填“吸热”或“放热”)反应。
②分析数据可知;人类不适合大规模模拟大气固氮的原因_____。
(2)NaNO2是一种食品添加剂(有毒性,市场上常误与食盐混淆)。可用酸性KMnO4溶液检验,完成其反应的离子方程式。MnO![]() +NO
+NO![]() +_____=Mn2++NO
+_____=Mn2++NO![]() +H2O。
+H2O。
(3)工业生产以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为: 2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(l) △H<0。T1℃时,在2 L的密闭容器中充入NH3和CO2模拟工业生产,若原料气中的NH3和CO2的物质的量之比(氨碳比)
CO(NH2)2(l)+H2O(l) △H<0。T1℃时,在2 L的密闭容器中充入NH3和CO2模拟工业生产,若原料气中的NH3和CO2的物质的量之比(氨碳比)![]() = x,如图是CO2平衡转化率(α)与氨碳比(x)的关系。
= x,如图是CO2平衡转化率(α)与氨碳比(x)的关系。
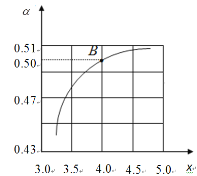
其它条件不变时,α随着x/span>增大而增大的原因是____;图中的B点处NH3的平衡转化率为____。
II.(4)红磷P(s)和Cl2 (g)发生反应生成PCl3(g)和 PCl5(g),反应过程如下。
2P(s) + 3Cl2(g)=2PCl3(g) △H1=-612 kJ· mol-1
2P(s) + 5Cl2(g)=2PCl5(g) △H2=-798 kJ· mol-1
气态PCl5生成气态PCl3和Cl2的热化学方程式为________。
(5)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x=___(用n表示)。
(6)一定温度下,向浓度均为0.20 mol·L-1的MgCl2和CaCl2混合溶液中逐滴加入Na3PO4,先生成__沉淀(填化学式);当测得溶液中钙离子沉淀完全(浓度小于10-5 mol·L-1)时,溶液中的另一种金属阳离子的物质的量浓度c = ______mol·L-1。(已知:Ksp[Mg3(PO4)2] =6.0×10-29,Ksp[Ca3(PO4)2]=6.0×10-26。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题给要求填空
(1)某元素的基态原子最外层电子排布式为3s23p2,它的次外层上电子云形状有________种,原子中所有电子占有________个轨道,核外共有________种运动状态不同的电子。
(2)E原子核外占有9个轨道,且具有1个未成对电子,E离子结构示意图是_______。
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,则G元素的原子序数是________,F2-的电子排布式是______。
(4)M能层上有________个能级,有________个轨道,作为内层最多可容纳________个电子,作为最外层时,最多可含有________个未成对电子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com