
| A. | C3H8只表示一种物质的分子组成 | |
| B. | C2H6的一氯代物只有1种 | |
| C. | C3H8O能与钠反应放出H2的同分异构体有3种 | |
| D. | 丙烷的二氯代物有4种 |
分析 A.分子式为C3H8的烷烃为丙烷,只有1种结构;
B.烃中含有几种等效氢原子,则一氯代物有几种;
C.C3H8O能与钠反应放出H2,说明含有羟基,C3H8分子中有2种化学环境不同的H原子,其一羟基代物有2种;
D.利用定一移二法确定二氯代物的同分异构体数目,写出一氯代物,再根据分子中含有H原子种类,判断二氯代物的数目.
解答 解:A.分子式为C3H8的丙烷,只有1种结构,结构简式为CH3CH2CH3,只表示一种物质的分子组成,故A正确;
B.C2H6的结构简式为CH3CH3,分子中只含有1种氢原子,一氯代物只有1种,故B正确;
C.C3H8O能与钠反应放出H2,说明含有羟基,C3H8分子中有2种化学环境不同的H原子,其一羟基代物有2种分别为:CH3CH2CH2OH和CH3CH(OH)CH3,故C错误;
D.丙烷分子中有2种H原子,其一氯代物有2种:CH3CH2CH2Cl,CH3CH(Cl)CH3,CH3CH2CH2Cl中含有3种H原子,再次一氯取代有3种产物:CH3CH(Cl)CH3中含有2种H原子,再次一氯取代有2种产物,其中有一种为同一物质,故丙烷的二氯代物有4种,故D正确;
故选C.
点评 本题考查同分异构体的书写,难度不大,注意体会利用定一移二法书写二元取代物.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
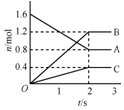 某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为2A?3B+C,2s内用A的浓度变化的平均反应速率为0.08mol/(L•s).
某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为2A?3B+C,2s内用A的浓度变化的平均反应速率为0.08mol/(L•s).查看答案和解析>>
科目:高中化学 来源: 题型:实验题
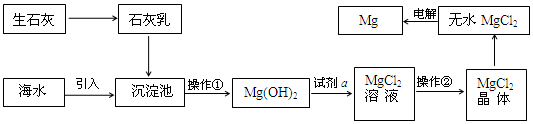
 海洋是巨大的资源宝库,从海洋中可获得淡水、单质碘、食盐等物质.
海洋是巨大的资源宝库,从海洋中可获得淡水、单质碘、食盐等物质.| 杂质 | CaCl2 | MgCl2 | Na2SO4 |
| 除杂试剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com