
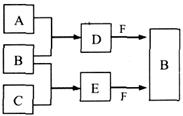
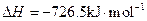 ,氢气的燃烧热
,氢气的燃烧热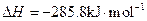 )
)科目:高中化学 来源:不详 题型:单选题
| A.干冰与二氧化硅晶体熔化时,所克服的微粒间相互作用不相同 |
| B.C2H5OH与C2H5Br相比,前者的相对分子质量远小于后者,而沸点却远高于后者,其原因是前者的分子间存在氢键 |
| C.非金属单质只能形成分子晶体 |
D.短周期元素离子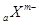 和 和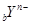 具有相同的电子层结构,若 具有相同的电子层结构,若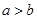 ,则 ,则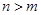 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.以非极性键结合起来的分子都是非极性分子 |
| B.以极性键结合起来的分子一定是极性分子 |
| C.极性分子中不可能有非极性键 |
| D.非极性分子中不可能有极性键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 为 。
为 。 4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为
4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为  ,每个Ba2+与 个O2-配位。
,每个Ba2+与 个O2-配位。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.①②③ | C.①②④ | D.①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com