
【题目】下列关于基本营养物质的说法不正确的是
A. 淀粉在人体内最终水解为葡萄糖
B. 蛋白质在人体内最终水解为氨基酸
C. 纤维素在人体内最终水解为葡萄糖
D. 油脂在人体内最终水解为甘油与高级脂肪酸
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】用石墨作电极电解KCl和CuSO4(等体积混合)混合溶液,电解过程中溶液pH随时间t的变化如图所示,下列说法正确的是
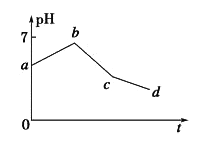
A. ab段H+被还原,溶液的pH 增大
B. cd 段相当于电解水
C. c点时加人适量CuCl2固体,电解液可恢复原来浓度
D. 原溶液中KCl和CuSO4的物质的量浓度之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以绿矾(FeSO4·7H2O)制备补血剂甘氨酸亚铁[(NH2CH2COO)2Fe] 有关物质性质如下:
甘氨酸(NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有强酸性和还原性 | 易溶于水,难溶于乙醇 |
实验过程:
Ⅰ.配制含0.10mol FeSO4的绿矾溶液。
Ⅱ.制备FeCO3:向配制好的绿矾溶液中,缓慢加入200mL 1.1mol·L-1NH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
Ⅲ.制备(NH2CH2COO)2Fe:实验装置如下图(夹持和加热仪器已省略),将实验Ⅱ得到的沉淀和含0.20 mol甘氨酸的水溶液混合后加入C中,然后利用A中的反应将C中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。
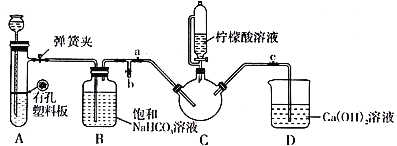
回答下列问题:
(1)实验I中:实验室配制绿矾溶液时,为防止FeSO4被氧化变质,应加入的试剂为_______(写化学式)。再滴加少量稀硫酸的作用是__________________________。
(2)实验II中:生成沉淀的离子方程式为__________________________。
(3)实验Ⅲ中:①C中盛柠檬酸溶液的仪器名称为___________________。
②装置A中所盛放的药品是___________________。(填序号)
A.Na2CO3和稀H2SO4 B.CaCO3和稀H2SO4 C.CaCO3和稀盐酸
③确认C中空气排尽的实验现象是____________________。
④加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是________________。
⑤洗涤实验Ⅲ中得到的沉淀,所选用的最佳洗涤试剂是___________________。(填序号)
A.热水 B.乙醇溶液 C.柠檬酸溶液
⑥若产品的质量为17.34g,则产率为________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在4℃时,100 mL水中溶解了 22.4 L HCl气体(标准状况下测得)后形成溶液。下列说法正确的是( )
A.该溶液物质的量浓度为10 mol/L
B.该溶液物质的量浓度因溶液的密度未知而无法求得
C.该溶液中溶质的质量分数因溶液的密度未知而无法求得
D.所得溶液的体积为22.5 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸是常用的干燥剂,根据需要可将浓硫酸配成不同浓度的稀硫酸。回答下列问题:
(1)![]()
![]() 的
的![]() 溶液中含有
溶液中含有![]() ______g,含有
______g,含有![]() ______个,将此溶液与足 量的铝片反应,生成的气体在标准状况下体积为______L。
______个,将此溶液与足 量的铝片反应,生成的气体在标准状况下体积为______L。
(2)配制上述稀硫酸需要量取质量分数为![]() ,密度为
,密度为![]() 的浓硫酸_____mL
的浓硫酸_____mL![]() 结果保留一位小数
结果保留一位小数![]() 。配制此溶液需要的玻璃仪器除了烧杯、玻璃棒、胶头滴管外还需要______________________________。
。配制此溶液需要的玻璃仪器除了烧杯、玻璃棒、胶头滴管外还需要______________________________。
(3)稀释浓硫酸的操作是_________________________________________________。
(4)下列操作使配制的硫酸溶液的物质的量浓度偏小的是______。
A.稀释浓硫酸时有液体溅出
B.容量瓶中有少量蒸馏水残留
C.浓硫酸稀释后溶液没有冷却到室温就转移
D.向容量瓶加水定容时仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识回答下列问题:
Ⅰ.丁腈橡胶(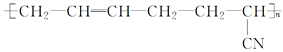 )具有优良的耐油、耐高温性能,合成丁腈橡胶的二种单体是_________________和_______________,是通过___________反应得到。
)具有优良的耐油、耐高温性能,合成丁腈橡胶的二种单体是_________________和_______________,是通过___________反应得到。
Ⅱ. 硅橡胶具有无毒,无味,耐高温又耐低温,可制成耐温垫圈,密封件和人造心脏,人造血管等,他是由单体二甲基二氯硅烷(CH3)2SiCl2水解得到二甲基硅二醇,经脱水缩聚成的聚硅氧烷再经交联制成的,请用化学方程式写出上述二甲基二氯硅烷水解及线性缩聚的方程式_________________和_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)同分异构现象在有机化合物中是非常普遍的。下列各组化合物:
①CH3CH2CH2CH3和(CH3)2CHCH3; ②CH3CH2OH和CH3CH2CH2OH;
③CH3COOCH2CH3和CH3CH2CH2COOH; ④CH3CH=CHCH3和CH3CH2CH=CH2;
⑤![]() 和
和![]() 。其中互为同分异构体的是______________________(填序号)。
。其中互为同分异构体的是______________________(填序号)。
(2)下列5种有机化合物:乙酸乙酯(CH3COOCH2CH3)、苯酚(![]() )、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
)、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
①其中能与Na2CO3溶液反应产生气泡的是______________________。
②其中能与FeCl3溶液发生显色反应的是________________________。
③其中能发生银镜反应的是________________________。
④写出乙酸乙酯碱性条件水解反应的化学方程式____________________________。
(3)①蛋白质是维持生命的重要物质,它是由_____________________通过缩聚反应生成的一类高分子化合物;氨基酸因分子中含有的官能团是____________________和____________________,而具有__________________性。
②2008年,三鹿婴幼儿奶粉由于人为添加三聚氰胺,导致长期食用该奶粉的部分婴幼儿出现肾结石病。三聚氰胺的结构简式如下图所示。
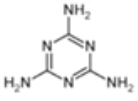
请你预测三聚氰胺在核磁共振氢谱图(1H核磁共振谱图)中会出现____________________个峰;三聚氰 胺中氮元素的质量分数为______________________(结果用百分数表示,并保留一位小数),添加三聚氰胺会使食品中蛋白质的含量虚高。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究过氧化钠的强氧化性,某研究性学习小组设计了如图所示的实验装置。
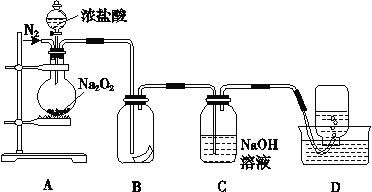
实验步骤及现象如下:
①检查装置气密性后,装入药品Na2O2并连接仪器。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸
入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,剧烈反应,产生黄绿色气体。
③一段时间后,将导管末端伸入集气瓶中收集气体。装置D中收集到能使带火星的木条复燃的无色气体。
④反应结束后,关闭分液漏斗的活塞,再通入一定量的N2,至装置中气体无色。
回答下列问题:
(1)装置B中湿润的红色纸条褪色,证明A中反应有______(填化学式)生成。若将B中红纸条改为湿润的紫石蕊试纸,现象为 _______
(2)实验前通N2的目的 ____,装置C的作用是_______
(3)甲同学认为O2是Na2O2被盐酸中的HCl还原所得。乙同学认为此结论不正确,其不赞成的理由可能为: ①_______;②O2有可能是Na2O2与盐酸中的H2O反应所得.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com