
 ),其过程如下:
),其过程如下: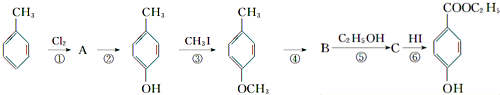
 .反应⑤是B与C2H5OH的反应,而最后的产物是对羟基苯甲酸乙酯(
.反应⑤是B与C2H5OH的反应,而最后的产物是对羟基苯甲酸乙酯( ),说明反应⑤是酯化反应;那么反应④是引入-COOH的反应,则B为
),说明反应⑤是酯化反应;那么反应④是引入-COOH的反应,则B为 ,C为
,C为 ,从④是氧化反应知,反应③和⑥的目的是保护酚羟基,防止被氧化.
,从④是氧化反应知,反应③和⑥的目的是保护酚羟基,防止被氧化. ,反应⑤是B与C2H5OH的反应,而最后的产物是对羟基苯甲酸乙酯(
,反应⑤是B与C2H5OH的反应,而最后的产物是对羟基苯甲酸乙酯( ),说明反应⑤是酯化反应;那么反应④是引入-COOH的反应,故B为
),说明反应⑤是酯化反应;那么反应④是引入-COOH的反应,故B为 ,C为
,C为 ,
, ;
; ;
; 与HI反应生成
与HI反应生成 与CH3I,反应方程式为:
与CH3I,反应方程式为: +HI→
+HI→ +CH3I,
+CH3I, +HI→
+HI→ +CH3I.
+CH3I.


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
| A、9.2mol/L |
| B、>9.2mol/L |
| C、<9.2 mol/L |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、8.1g |
| B、5.4g |
| C、3.6 g |
| D、2.7g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
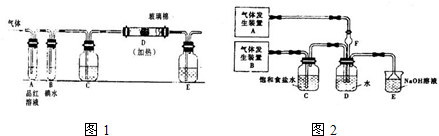
查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子 | Cu2+ | Al3+ | NO3- | Cl- |
| 1 | 1 | a | 1 |
| A、阴极析出的金属是铜与铝 |
| B、a=3 |
| C、阳极生成1.5 mol Cl2 |
| D、电解后溶液的pH=0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com