
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
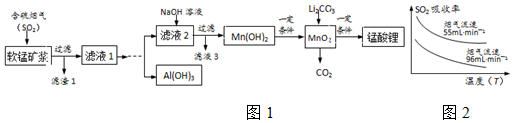
分析 软锰矿浆(主要成分为MnO2,含少量Fe2O3、FeO、Al2O3、SiO2制备锰酸锂,在实际生产中,Li2CO3与MnO2按物质的量之比为1:4混合均匀加热制取LiMn2O4.软锰矿浆通入含二氧化硫的烟气,二氧化硫溶于水生成亚硫酸,MnO2、Fe2O3、FeO、Al2O3、都能溶于酸,二氧化硅不溶盐酸,滤渣1为二氧化硅,滤液1含Al3+、Mn2+、Fe2+,滴加足量过氧化氢,搅拌加入氢氧化钠溶液至4.7≤PH<7.7,过滤得到滤液2和固体向所得固体中加入氢氧化钠溶液至PH≥12,搅拌过滤再向所得滤液中通入二氧化碳过滤洗涤,低温烘干得到氢氧化铝,滤液2中加入氢氧化钠溶液过滤得到Mn(OH)2,一定条件下得到MnO2,Li2CO3与MnO2按物质的量之比为1:4混合均匀加热制取LiMn2O4.
(1)图象分析可知随温度升高,二氧化硫的吸收率降低;
(2)烟气中含二氧化硫溶于水生成亚硫酸,溶液显酸性,二氧化硅是酸性氧化物不与亚硫酸反应,氧化铝是两性氢氧化物,氧化铁和氧化亚铁是碱性氧化物,且铁离子具有氧化性把二氧化硫以为硫酸本身被还原为亚铁离子,二氧化锰中+4价锰被还原为Mn2+;
(3)①考虑二氧化锰的催化剂作用;
②升温到566℃时,MnO2开始分解产生另一种气体X只能为氧气,氧气恰好与①中产生的CO2物质的量相等,假设Li2CO3的物质的量为1mol,MnO2物质的量为4mol,则产生1molCO2即生成1molO2,元素守恒B中含4molMn和6molO,同时得到固体B的化学式Mn2O3;
③升温到720℃时,A、B反应,固体质量逐渐增加,当质量不再增加时,得到高纯度的锰酸锂,Li2O和Mn2O3反应生成LiMn2O4;
(4)依据(2)分析含有的离子是Al3+、Fe2+等,根据流程图锰离子存在在溶液中,需要把铁离子和铝离子沉淀不能影响锰离子表中数据分析,把亚铁以为铁离子,然后调节溶液PH,使铁离子、铝离子完全沉淀,再利用氢氧化铝的两性除去氢氧化铁;
解答 解:(1)图象分析可知随温度升高,二氧化硫的吸收率降低,因此提高二氧化硫吸收率需要降低通入含硫烟气的温度或减小通入含硫烟气的流速,
故答案为:降低通入含硫烟气的温度或减小通入含硫烟气的流速;
(2)烟气中含二氧化硫溶于水生成亚硫酸,溶液显酸性,二氧化硅是酸性氧化物不与亚硫酸反应,氧化铝是两性氢氧化物,氧化铁和氧化亚铁是碱性氧化物,且铁离子具有氧化性把二氧化硫以为硫酸本身被还原为亚铁离子,二氧化锰中+4价锰被还原为Mn2+,因此滤液1中含有的金属阳离子是Al3+、Mn2+、Fe2+,
故答案为:Al3+、Fe2+;
(3)①升温到515℃时,Li2CO3开始分解产生CO2,同时生成固体A,此时比预计Li2CO3的分解温度(723℃)低得多,说明MnO2对Li2CO3的分解有催化剂的作用,
故答案为:MnO2对Li2CO3的分解有催化剂的作用;
②升温到566℃时,MnO2开始分解产生另一种气体X只能为氧气,氧气恰好与①中产生的CO2物质的量相等,假设Li2CO3的物质的量为1mol,MnO2物质的量为4mol,则产生1molCO2即生成1molO2,元素守恒B中含4molMn和6molO,同时得到固体B的化学式Mn2O3,反应的化学方程式为:4MnO2 $\frac{\underline{\;566℃\;}}{\;}$ 2Mn2O3+O2↑,
故答案为:4MnO2 $\frac{\underline{\;566℃\;}}{\;}$ 2Mn2O3+O2↑;
③升温到720℃时,A、B反应,固体质量逐渐增加,当质量不再增加时,得到高纯度的锰酸锂,Li2O和Mn2O3反应生成LiMn2O4,因为固体质量增加,反应的化学方程式为:2Li2O+4Mn2O3+O2$\frac{\underline{\;720℃\;}}{\;}$4LiMn2O4,
故答案为:2Li2O+4Mn2O3+O2$\frac{\underline{\;720℃\;}}{\;}$4LiMn2O4;
(4)依据(2)分析含有的离子是Al3+、Fe2+等,根据流程图锰离子存在在溶液中,需要把铁离子和铝离子沉淀不能影响锰离子表中数据分析,把亚铁以为铁离子,然后调节溶液PH,使铁离子、铝离子完全沉淀,再利用氢氧化铝的两性除去氢氧化铁,具体步骤为:滴加足量过氧化氢,搅拌加入氢氧化钠溶液至4.7≤PH<7.7,过滤得到滤液2和固体向所得固体中加入氢氧化钠溶液至PH≥12,搅拌过滤再向所得滤液中通入二氧化碳过滤洗涤,低温烘干得到氢氧化铝;
点评 本题考查了物质分离提纯的过程分析判断、物质性质转化,除杂方法的利用、反应化学方程式书写、实验设计等,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
| 热化学方程式 | 平衡常数 | |
| ① | 2NO2(g)+NaCl(s)?NaNO3(s)+NOCl(g)△H1 | K1 |
| ② | 4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g)△H2 | K2 |
| ③ | 2NO(g)+Cl2(g)?2NOCl(g)△H3 | K3 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在稀氨水中,丁二酮肟(CH3C=N-OH)2与Ni2+反应可生成鲜红色沉淀丁二酮肟镍(结构如图),常用于检验Ni2+.
在稀氨水中,丁二酮肟(CH3C=N-OH)2与Ni2+反应可生成鲜红色沉淀丁二酮肟镍(结构如图),常用于检验Ni2+.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定温度下,某可逆反应在某体积为5L的密闭容器中进行,在从0-3分钟各物质的量的变化情况如图所示(A,B,C均为气体)
一定温度下,某可逆反应在某体积为5L的密闭容器中进行,在从0-3分钟各物质的量的变化情况如图所示(A,B,C均为气体)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
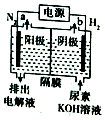 用如图所示的装置,采用廉价的镍催化剂,通过电化学方法,可在碱性环境中直接使尿素转化成纯氢,电极为惰性电极,隔膜仅阻止气体通过,下列相关叙述不正确的是( )
用如图所示的装置,采用廉价的镍催化剂,通过电化学方法,可在碱性环境中直接使尿素转化成纯氢,电极为惰性电极,隔膜仅阻止气体通过,下列相关叙述不正确的是( )| A. | 尿素由碳、氮、氧、氢四种元素组成的有机化合物 | |
| B. | 尿素在阳极被氧化,当生成1 mol N2时,转移电子为6 mol | |
| C. | a、b两处生成的气体体积比为1:3 | |
| D. | 假设电解过程中溶液体积不变,电解后排出液的pH比通入前大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )
t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )| A. | 在t℃时,AgBr的Ksp为4.9×10-13 | |
| B. | 通过蒸发,可使溶液由a点变到c点 | |
| C. | 图中b点有AgBr沉淀析出 | |
| D. | 在t℃时,AgCl(s)+Br-(aq)?AgBr(s)+Cl-(aq)的平衡常数K≈816 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在一定温度下,容器内某一反应中 M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中 M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A. | t3时,逆反应速率大于正反应速率 | |
| B. | t2时,正逆反应速率相等,反应达到平衡状态 | |
| C. | t1时,N 的浓度是 M 浓度的 2 倍 | |
| D. | 反应的化学方程式为:2M?N |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com