

分析 (1)原电池中,正极发生还原反应,负极发生氧化反应,投入氧气的一极为正极,负极甲醚失电子被氧化生成碳酸根离子;
(2)铁电极连接原电池的负极,为电解池的阴极,石墨为阳极,氯离子放电被氧化生成氯气;
(3)活泼性Zn>Cu>Ag,阳极上锌、铜被氧化;
(4)据串联电池中转移电子数相等得氧气、氢气和铜的关系式为:O2----2H2----2Cu计算;根据转移电子数相等计算乙装置中阳离子交换膜左侧溶液质量变化;
(5)若将乙装置中铁电极与石墨电极位置互换,Fe作阳极失电子生成亚铁离子,阴极上氢离子得电子生成氢气.
解答 解:(1)燃料电池是将化学能转变为电能的装置,属于原电池,投放燃料的电极是负极,投放氧化剂的电极是正极,所以通入氧气的电极是正极,负极上甲醚失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH3OCH3-12e-+16OH-═2CO32-+11H2O,
故答案为:CH3OCH3-12e-+16OH-═2CO32-+11H2O;
(2)乙池有外接电源属于电解池,铁电极连接原电池的负极,所以是阴极,则石墨电极是阳极,阳极上氯离子放电生成氯气,电极反应式为:2Cl--2e-═Cl2↑,
故答案为:阴;2Cl--2e-═Cl2↑;
(3)如果粗铜中含有锌、银等杂质,阳极上不仅铜还有锌、银失电子进入溶液,阴极上析出铜离子,阳极电极方程式分别为Zn-2e-=Zn2+、Cu-2e-=Cu2+,根据转移电子数相等知,阳极上溶解的铜小于阴极上析出的铜,所以丙装置中反应一段时间,硫酸铜溶液浓度将减小,
故答案为:减小;
(4)根据串联电池中转移电子数相等得氧气、氢气和铜的关系式为:O2----2H2----2Cu,设生成氢气的分子数是x,生成铜的质量是y.
O2------2H2 -------2Cu
22.4L 128g
2.24L x
x=12.8g,
根据串联电池中转移电子数相等得氧气、氢气的关系式为:O2----2H2,设生成氢气的物质的量是xmol,
O2 -------2H2
22.4L 2
0.224L x
x=0.02,所以消耗0.02×2=0.04mol氢离子,则乙装置中阳离子交换膜右侧进入左侧的钠离子也为0.04mol,所以乙装置中阳离子交换膜左侧溶液质量将增大0.04×23-0.04×1=0.88g
故答案为:12.8 g;增大;0.88;
(5)若将乙装置中铁电极与石墨电极位置互换,Fe作阳极失电子生成亚铁离子,阴极上氢离子得电子生成氢气,则电解总方程式为Fe+2H2O$\frac{\underline{\;通电\;}}{\;}$ Fe(OH)2↓+H2↑;
故答案为:Fe+2H2O$\frac{\underline{\;通电\;}}{\;}$ Fe(OH)2↓+H2↑.
点评 本题考查原电池和电解池知识,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意把握电极方程式的书写,为解答该题的关键,结合串联电路的特点解答该题,难度中等.


 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:填空题
| 阳离子 | Na+,Ba2+,NH4+ |
| 阴离子 | CH3COO-,Cl-,OH-,SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 编号 | 改变的条件 | 生成的SO3的速率 |
| ① | 降低温度 | 减小 |
| ② | 升高温度 | 增大 |
| ③ | 增大O2的浓度 | 增大 |
| ④ | 恒容下充入Ne | 不变 |
| ⑤ | 压缩体积 | 增大 |
| ⑥ | 使用催化剂 | 增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
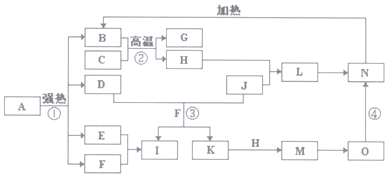
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2、 | B. | CH4、CH3CH2CH3 | ||
| C. | C2H2、C6H6 | D. | CH3-O-CH3、CH3-OH |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 离子(0.1mol/L) | Cu2+ | Fe2+ | Fe3+ | 提供的药品(根据需要选择使用) |
| 氢氧化物开始沉淀pH | 4.7 | 7.0 | 1.9 | Cl2、NaOH溶液、CuO、Cu |
| 氢氧化物沉淀完全pH | 6.7 | 9.0 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | LiOH、KOH、CsOH的碱性依次增强 | B. | H2O、NH3、PH3的热稳定性依次增强 | ||
| C. | HCl、HBr、HI的还原性依次减弱 | D. | Na、Mg、Al的原子半径依次增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 从海水中可提取食盐 | |
| B. | 海水蒸馏可得淡水 | |
| C. | 直接电解海水可得镁 | |
| D. | 从海水中得到淡水的方法有蒸馏法、电渗析法、离子交换法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 研究NOX和CO等的处理方法对环境保护有重要意义.
研究NOX和CO等的处理方法对环境保护有重要意义. ①计算0~4分钟在A催化剂作用下,反应速率v(NH3)=0.25mol/(L•min).
①计算0~4分钟在A催化剂作用下,反应速率v(NH3)=0.25mol/(L•min).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com