
����Ŀ��һ�������£���ij�ܱ������м���һ������N2��H2�������淴Ӧ:N2(g)+3H2(g)![]() 2NH3(g) ��H = -92.2kJmol��1�����0��10���ڣ�c(H2)��С��0.75molL��1������˵����ȷ����( )
2NH3(g) ��H = -92.2kJmol��1�����0��10���ڣ�c(H2)��С��0.75molL��1������˵����ȷ����( )
A��10��15����c(NH3) ����������0.25mol L��1
B��10���ڰ�����ƽ����Ӧ����Ϊ0.025molL��1��s��1
C����ƽ����������NH3,v�� ����
D���÷�Ӧ���淴Ӧ�Ļ�ܲ�С��92.2kJmol��1
���𰸡�D
��������
���������A��0��10���ڣ�c(H2)��С��0.75molL��1��c(NH3)��Ũ��������0.5mol/L�����ŷ�Ӧ�Ľ��У���Ӧ���Ũ�ȼ�С����Ӧ���ʼ�С������10s��15s��c��NH3��������С��0.25mol/L��A�����B�����0��10s�ڣ�c��H2����С��0.75mol/L����c��NH3��������0.5mol/L������10s�ڰ�����ƽ����Ӧ����Ϊ��0.5mol/L��10s=0.05molL-1s-1��B�����C�������������Ũ�ȣ���Ӧ���ʼ�С�����ƽ����������NH3��ƽ��������Ӧ�����ƶ���v����С��C�����D����֪N2��g��+3H2��g��![]() 2NH3��g����H=-92.2kJmol-1����H=����Ӧ�Ļ��-�淴Ӧ�Ļ��=-92.2kJmol-1�����淴Ӧ�Ļ��=����Ӧ�Ļ��+92.2kJmol-1�������淴Ӧ�Ļ�ܲ�С��92.2kJmol-1��D����ȷ����ѡD��
2NH3��g����H=-92.2kJmol-1����H=����Ӧ�Ļ��-�淴Ӧ�Ļ��=-92.2kJmol-1�����淴Ӧ�Ļ��=����Ӧ�Ļ��+92.2kJmol-1�������淴Ӧ�Ļ�ܲ�С��92.2kJmol-1��D����ȷ����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ȡ���Һ��Ͻ��еIJ���(��CCl4Ϊ��ȡ�����ӵ�ˮ����ȡ��)�д������(����)
A�����͵�ˮ��CCl4�����Һ©���к������Ͽڲ������ӣ���һ��ѹס��Һ©���Ͽڲ���һ����ס�������֣��ѷ�Һ©����ת������
B�����ã�����Һ©����Һ��ֲ����ʹ��Һ©�����������ͨ(���ų�Һ��)
C����Һ©���Ļ�����ʹȫ���²�Һ���سн�Һ����ձ��ڱ���������
D�����������������������нӲ������ϲ�Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ߴ����������й㷺����;��ij�о�С��������������ȡ�ߴ�����������
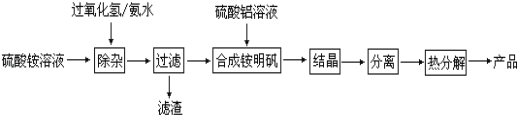
������������ͼ��գ�
��1�������ӡ��������ȼ�����������ַ�Ӧ�����ð�ˮ������Һ��pH��ʹ�������Һ�е�����Fe2+����ΪFe3+����һ��ת��ΪFe(OH)3�Ӷ���ȥFe2+����Fe2+��������������ΪFe3+�����ӷ���ʽΪ:
��2��������������Һʱ�����������ữ���ữ��Ŀ���� ��
��3�������롱������������ ������ĸ���ţ���
A������ B����Һ C������
��4�����������Ļ�ѧʽΪNH4Al��SO4��212H2O����������� ����������������0.1mol/L�������ˮ��Һ�У�Ũ������������ ��
��5���ȷֽ��з������·�Ӧ6NH4Al(SO4)2 = 3Al2O3 + 2NH3 ��+ 2N2 ��+ 6SO2 ��+ 6SO3 ��+ 9H2O,������1mol Al2O3ʱת�Ƶ������ʵ���Ϊ mol
��6������0.1mol�����ϡ��Һ����μ��뺬0.3mol Ba(OH)2��ϡ��Һ,��Ӧ�������ӷ���ʽΪ: ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ�ý���ʵ�飬��ʼʱ��a��b����Һ����ƽ���ܷ�ã�����һ��ʱ�䡣����˵������ȷ����( )
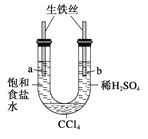
A��a�ܷ���������ʴ��b�ܷ������ⸯʴ
B��һ��ʱ���a��Һ�����b��Һ��
C��a����Һ��pH����b����Һ��pH��С
D��a��b����������ͬ�ĵ缫��Ӧʽ��Fe��2e��===Fe2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijǿ������Һ�к���Fe3+��Mg2+���ڴ���Һ�л��ܴ��ڵ���������( )
A��K+��Na+��HC03-��S042- B��OH-��K+��Cu2+��NO3-
C��K+��SCN-��I-��Na+ D��K+��SO42-��Na+��NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ú�̼������ϳ�ȼ���ǽ����ԴΣ������Ҫ��������֪CO(g)��2H2(g)![]() CH3OH(g)��Ӧ�����е������仯�����ͼ��ʾ�����ߢ�����ߢ�ֱ��ʾ��ʹ�ô�����ʹ�ô�������������������ж���ȷ���� ( )
CH3OH(g)��Ӧ�����е������仯�����ͼ��ʾ�����ߢ�����ߢ�ֱ��ʾ��ʹ�ô�����ʹ�ô�������������������ж���ȷ���� ( )
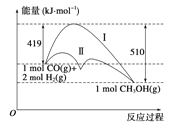
A���÷�Ӧ�Ħ�H����91 kJ��mol��1
B������������÷�Ӧ�Ħ�H��С
C����Ӧ���������С���������������
D������÷�Ӧ����Һ̬CH3OH����H��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������أ�����˵����ȷ����
A. �������ֿ���ʳƷ���ʼ�
B. ����ȼ�ջ�ʯȼ�����������������һ����Ҫԭ��
C. ��ȼ�������ȼ������SO3
D. �þ���ϩ���ϴ�����������Ͽɼ��ٰ�ɫ��Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йع�ҵ�����������У�����ȷ������
A. ���������ʱ���ñ���ʯ�������۵� B. �Ʋ���ʱ���������������Խ��������ɱ�
C. ���ӱ�Ҫ��Ԫ�ؿ���߸ֲĵ����� D. ���ѻ���������͵IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������X�ķ���ʽΪC5H11Cl����NaOH�Ĵ���Һ����X���ɵ÷���ʽΪC5H10�����ֲ���Y��Z��Y��Z��������ɵõ�2�����顣����������X��NaOH��ˮ��Һ�������������л�����Ľṹ��ʽ�������� ��
A��CH3CH2CH2CH2CH2OH B����CH3��2COHCH2CH3
C����CH3��2CHCH2CH2OH D����CH3��3CCH2OH
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com