
分析 先根据化学式ACl2计算出ACl2的物质的量,然后根据M=$\frac{m}{n}$计算出ACl2的摩尔质量;根据摩尔质量与相对分子质量的关系可确定A的相对原子质量,从而可确定A的名称,最后写出ACl2的化学式.
解答 解:27.2g某二价金属氯化物(ACl2)中含有0.4molCl-,则n(ACl2)=$\frac{1}{2}$n(Cl-)=0.4mol×$\frac{1}{2}$=0.2mol,则ACl2的摩尔质量是:$\frac{27.2g}{0.2mol}$=136g/mol,ACl2的相对分子质量为136,A的相对原子质量为:136-35.5×2=65,则A为Zn,ACl2的化学式是ZnCl2,
故答案为:136g/mol;65;ZnCl2.
点评 本题考查了物质的量的计算,题目难度不大,明确摩尔质量与相对分子质量之间的关系为解答关键,注意掌握物质的量与摩尔质量之间的关系,试题培养了学生的化学计算能力.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案科目:高中化学 来源: 题型:实验题
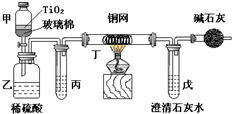 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑧ | B. | ③⑥⑨⑩ | C. | ④⑤⑧⑨ | D. | ④⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 弱电解质的导电能力一定比强电解质的导电能力弱 | |
| B. | pH=4的醋酸与pH=10的NaOH溶液等体积混合后溶液显碱性 | |
| C. | 豆浆中加入硫酸钙会使蛋白质聚沉. | |
| D. | 同浓度的①NaHCO3②Na2CO3③CH3COONa四种溶液,pH值大小排列顺序是②>①>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 +Br2→BrCH2CH2CH2CH2CH2Br
+Br2→BrCH2CH2CH2CH2CH2Br
| A. | 环烷烃与烷烃都是饱和烃,所以具有相同的通式 | |
| B. | B所有的饱和烃都不能发生加成反应 | |
| C. | 可用溴水鉴别丙烯与环丙烷 | |
| D. | 可用酸性高锰酸钾溶液鉴别丙烯与环丙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 伴有能量变化的物质变化不一定都是化学反应 | |
| C. | 在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同 | |
| D. | 在一个确定的化学反应关系中,反应物的总能量总是大于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由2H和18O所组成水22g,其中所含的中子数为11NA | |
| B. | 分子数为NA的N2、CO混合气体体积为22.4L,质量为28g | |
| C. | 标准状况下,22.4LNO和11.2LO2混合后气体的原子总数为3NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 共价键 | 键能 | 共价键 | 键能 |
| H-H | 436 | H-F | 565 |
| C-F | 427 | H-S | 339 |
| C-Cl | 330 | H-Se | 314 |
| A. | H2(g)→2H (g)-436kJ | |
| B. | 键长越短,共价键越牢固 | |
| C. | 相同条件下CH3F比CH3Cl更 易发生水解反应 | |
| D. | 相同压强下,H2S的沸点比 H2Se的沸点高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com