
【题目】取50.0mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66g,并有气体放出,试计算:
(1)原混合液中CO32-的物质的量浓度为,Na+的物质的量浓度为。
(2)产生的气体在标准状况下的体积L。
【答案】
(1)1mol/L;2.8mol/L;
(2)1.12;
【解析】
试题分析:(1)14.51克白色沉淀是BaCO3和BaSO4混合物,剩余沉淀为BaSO4,Na2SO4的物质的量等同于BaSO4的物质的量所以Na2SO4的物质的量为:![]() =0.02mol,减少的沉淀质量为BaCO3,Na2CO3的物质的量等同于BaCO3的物质的量所以Na2CO3的物质的量为:
=0.02mol,减少的沉淀质量为BaCO3,Na2CO3的物质的量等同于BaCO3的物质的量所以Na2CO3的物质的量为:![]() =0.05mol,所以Na2CO3的物质的量浓度为
=0.05mol,所以Na2CO3的物质的量浓度为![]() =1mol/L,则Na+的物质的量浓度为
=1mol/L,则Na+的物质的量浓度为![]() =2.8mol/L,答:原混和溶液中Na2CO3和Na2SO4的物质的量浓度分别为:1mol/L、2.8mol/L;
=2.8mol/L,答:原混和溶液中Na2CO3和Na2SO4的物质的量浓度分别为:1mol/L、2.8mol/L;
(2)设生成的气体在标准状况下的体积为x.
BaCO3+2HNO3═Ba(NO3)2+H2O+CO2↑
1mol22.4L
0.05molx
![]() =
=![]() ,x=1.12L,答:产生的气体在标准状况下的体积为1.12L.
,x=1.12L,答:产生的气体在标准状况下的体积为1.12L.


科目:高中化学 来源: 题型:
【题目】下列解释事实的化学方程式或离子方程式不正确的是
A.工业上可用电解法制备Mg:MgCl2(熔融)![]() Mg+Cl2↑
Mg+Cl2↑
B.用FeSO4除去酸性废水中的Cr2O72-:Cr2O72-+Fe2++14H+=2Cr3++Fe3++7H2O
C.用CaSO4治理盐碱地:CaSO4(s)+Na2CO3(aq)![]() CaCO3(s)+Na2SO4(aq)
CaCO3(s)+Na2SO4(aq)
D.向Ca(ClO)2溶液中通入少量CO2:Ca2++2C1O-+H2O+CO2=2HC1O+CaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属(M)–空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH) n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是( )

A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B.比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高
C.在M–空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
D.M–空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
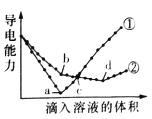
下列分析不正确的是( )
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH-
C.c点,两溶液中含有相同量的OH-
D.a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解CuSO4和NaCl的混合溶液,开始时阴极和阳极上分别析出的物质是
A.H2和Cl2 B.Cu和Cl2 C.H2和O2 D.Cu和O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有①Na+ 、②Ba2 +、 ③Cl一、 ④Br一、⑤SO32一、⑥SO42一 离子中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下。

下列结论不正确的是( )
A.肯定没有的离子是② B.不能确定的离子是③⑥
C.肯定含有的离子是①③④⑤ D.肯定含有的离子是①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列说法正确的是( )
A.将pH=2的酸溶液稀释10倍,溶液的pH一定变为3
B.将pH=2的盐酸溶液和pH=4的盐酸溶液等体积混合后,溶滚的pH变为3
C.将pH=12的Ba(OH)2溶液稀释10倍,溶液的pH变为13
D.将pH=a的盐酸与pH=b的NaOH溶液等体积混合后,若pH=7, 则a+b=14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 化学反应中的能量变化都表现为热量的变化
B. 需要加热才能发生的反应一定是吸热反应
C. 放热反应在常温下一定很容易发生
D. 反应是吸热还是放热必须看反应物和生成物的总能量的大小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com