
A.工业制漂白粉通常是将氯气与石灰乳反应而不是与澄清石灰水反应
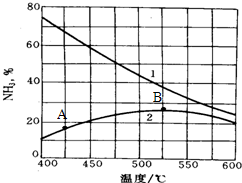
B.硫酸工业中,SO2氧化成SO3时,为了提高SO2的转化率通常采用高压条件
C.合成氨工业中使用催化剂,能促使平衡N2+3H2![]() 2NH3向正方向移动
2NH3向正方向移动
D.氨碱工业中,阳极发生氧化反应生成了H2和NaOH
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
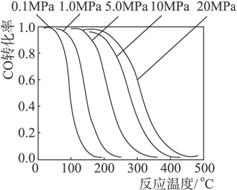
下列关于新法和旧法的说法正确的是
A.旧法生产中,由图知CO与H2合成甲醇的反应属于放热反应
B.旧法生产中,选择合适催化剂时,可推测高压法合成比低压法合成更有发展优势
C.新法与旧法相比,原料丰富并可直接从天然气中获得
D.新法生产中,需控制V(CH4)/V(O2)=9∶1,目的是提高空气中氧气的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(12分)绿色化学是当今社会人们提出的一个新概念,它可以公开为环境友好化学。它的核心内涵是在反应过程中和化工生产中,尽量减少或彻底消除使用和产生有害物质。这就是说,绿色化学的着眼点是使污染消灭在生产的源头,从根本上消除污染。1995年,美用总统克林顿首次设立“总统绿色化学挑战奖”,目的是鼓励、促进化学家们设计、改进化学产品和化工生产过程,使其对环境更加友好,企业经济效益得到更大的提高。为此,美国斯坦福大学Barry Trost教授提出了绿色化学下的原子经济的概念。最理想的原子经济是全部反应物的原子嵌入期望的最终产物中,不产生任何废弃物,这时的原子经济百分数便是100%。原子经济百分数的计算公式为:
![]()
例如:Claisen分子重排反应:
反应过程中只是改变了分子内部部分原子的连接方式,所有的反应物的原子全部并入最终产物中,所以这是一个100%的原子经济反应。
根据上述材料回答下列有关问题。
1.下面叙述错误的是_________(填编号,下同)。
①绿色化学和环境化学都是研究环境保护和治理的
②绿色化学不是被动的治理环境,而是主动地防止环境污染
③绿色化学保护了环境,而且也能给有关企业带来巨大的经济利益
2.硝酸工业的尾气中主要含NO、NO2气体。下列关于它们的危害的叙述中,正确的是_______________。①形成酸雨 ②破坏臭氧层 ③NO能刺激呼吸道 ④NO2能跟血红蛋白作用生成二氧化氮血红蛋白而引起中毒 ⑤NO、NO2在空气中形成褐色或黄色的毒性很大的烟雾。
工厂里常采用NaOH溶液吸收NO、NO2,使其转化为化工产品NaNO2,请写出其化学反应方程式
这一处理方法是否符合绿色化学概念__________(填“是”或“不是”)。其原子经济百分数为 。
3.有人采用下面两种方法制取Cu (NO3)2。
①方法一:2Cu+O2![]() 2CuO CuO+2HNO3(稀)=Cu(NO3)2+H2O
2CuO CuO+2HNO3(稀)=Cu(NO3)2+H2O
②方法二;3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
其中符合绿色化学概念的方法是________________。
4.有人将3中反应②产生的NO收集到一个固定容积的密闭容器中,并在常温下将其压缩到1.01×107 Pa,然后加热至50℃时,发现气体的压力迅速下降。当温度恢复到常温,压强降至略小于1.01×107 Pa的2/3时,就不再改变。已知此过程中有一种产物是N2O。请写出生成N2O的反应方程式:
解释最后的气体压强略小于1.01×107 Pa的2/3原因:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com