
【题目】常温下,已知:铝热反应放热,①4Al(s)+3O2(g)=2Al2O3(s) H1②4Fe(s)+3O2(g)===2Fe2O3(s) H2 下面关于 H1、H2 的比较正确的是( )
A. H1<H2 B. H1=H2 C. H1>H2 D. 无法判断
科目:高中化学 来源: 题型:
【题目】重铬酸钠晶体俗称红矾钠,是重要的化工产品和强氧化剂。工业上用含有Al2O3、Fe2O3等杂质的铬铁矿【主要成份为Fe(CrO2)2】为主要原料生产重铭酸钠晶体(Na2Cr2O7·2H2O)的主要工艺流程如下:
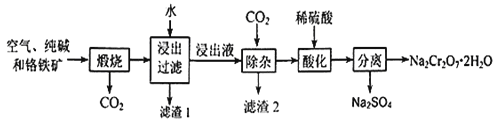
已知:铬铁矿在空气中与纯碱煅烧生成Na2CrO4和一种红棕色固体,放出CO2气体,同时发生反应:A12O3+Na2CO3![]() 2NaAlO2+CO2↑。请回答下列问题:
2NaAlO2+CO2↑。请回答下列问题:
(1)煅烧前通常将铬铁矿粉碎,原因是 。
(2)化学上可将某些盐写成氧化物的形式,如Na2SiO3可写成Na2O·SiO2,则Fe(CrO2)2可写成 。
(3)滤渣2的成分为 (填写化学式)
(4)请写出用稀硫酸酸化处理时发生反应的离子方程式 、 。
(5)称取重铬酸钠晶体试样2.500g配成250ml溶液,取出25ml于锥形瓶中,加入10mL 2mol/ LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放置于暗处5min。然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)
①判断滴定达到终点的现象是 ;
②若实验中共用去Na2S2O3标准溶液40.00ml,则所得产品Na2Cr2O7·2H2O的纯度为 (设整个过程中其它杂质不参加反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用浓盐酸配制l∶l(体积比)的稀盐酸(约6mol/L)100mL,应选用的定量仪器
A. 量筒 B. 滴定管 C. 50mL容量瓶 D. 100mL容量瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO很容易与许多分子迅速发生反应,科学家发现在生命体中会不断地产生NO,用于在细胞和细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
(1)、实验室用金属铜和稀硝酸制取NO的化学方程式:________________。
最适宜的收集方法是( )


(2)、NO是有毒气体,某学生为防止污染,用分液漏斗和 烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图所示。实验室用小铜粒做实验,在使用上述装置进行实验时,可用丝状材料包裹铜粒进行,这丝状材料的成分可以是________________(填选项编号)
A.铁 B.铝 C.玻璃
用丝状材料包裹的原因是__________________。
(3)、将(2)题图中分液漏斗的活塞打开,使反应进行,在分液漏斗中看到________色气体。原因是(填化学方程式):__________________。
(4)、为证明铜丝与稀硝酸反应生成的确实是NO,某同学另设计了一套如图所示制取NO的装置。
在带有铜丝的塞子插入硝酸的同时拔去左边的塞子,反应发生,再过一段时间后发现反应会自动停止,其原因是____________________。
(5)、在(4)题反应结束后右管上端可以看到有一段无色气体,为了验证该气体为NO,能否将带铜丝的塞子拔去?__________(能、不能),理由是_________________。
(6)、若带铜丝的塞子不拔去,将左管的塞子塞上后,只需一个简单的操作即可验证无色气体为NO,该操作是_________________;过一段时间后,气体颜色慢慢变浅,其原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列有关图象,说法正确的是( )
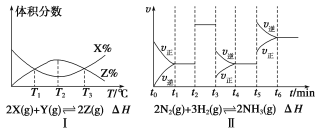

①由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的ΔH<0
②由图Ⅱ知,反应在t6时刻,NH3体积分数最大
③由图Ⅱ知,t3时采取减小反应体系压强的措施
④图Ⅲ表示在10 L容器、850 ℃时的反应,由图知,到4 min 时,反应放出51.6 kJ的热量
A.①③ B.②④ C.③④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物环丙叉环丙烷,由于其特殊的电子结构一直受到理论化学家的注意,右下图是它的结构示意图。下列关于环丙叉环丙烷的有关说法中错误的是( )

A.环丙叉环丙烷的二氯取代物有4种
B.环丙叉环丙烷不是环丙烷的同系物
C. 环丙叉环丙烷所有的原子均在同一平面内
D. 环丙叉环丙烷与环己二烯互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500 mL NaNO3和Cu(NO3)2的混合溶液中c(NO![]() )=6 mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到气体22.4 L(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
)=6 mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到气体22.4 L(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
A.原混合溶液中c(Na+)=6 mol
B.电解后得到的Cu的物质的量为2 mol
C.上述电解过程中共转移8 mol电子
D.电解后溶液中c(H+)=4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】直接排放含SO2的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关SO2性质的探究活动。

(1)装置A中反应的离子方程式为 。
(2)选用图1以上装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按照A→C→F→尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是 。
②丙同学设计的合理实验方案为:按照A→C →尾气处理(填字母)顺序连接装置。其中装置C的作用是 。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是 。
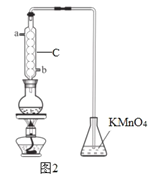
(3)利用如图2的装置A测残液中SO2的含量。量取10.00 mL残液于圆底烧瓶中,加热使SO2全部蒸出,用20.00 mL 0.1000 mol/L的KMnO4标准溶液吸收。充分反应后,再用0.2000 mol/L的KI溶液滴定过量的KMnO4,消耗KI溶液25.00 mL。
(已知:5SO2+2MnO4-+2H2O==2Mn2++5SO42-+4H+,10I-+2MnO4-+16H+==2Mn2++5I2+8H2O)
①该装置中仪器C的名称为 ,水通入C的进口为_____________。
②残液中SO2的含量为 mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com