
【题目】某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。

(1)加入的试剂①为______(填化学式),加入试剂①的目的____________________。
(2)操作a的名称为过滤、洗涤,所需要的玻璃仪器为______。
(3)加入的试剂③为_______(填化学式),发生的离子反应方程式为___________________________________________________。
(4)固体E的成分为_____(填化学式),加入的试剂④为_____(填化学式),发生的离子反应方程式为___________________________________________。
(5))从溶液D和溶液G中得到FeSO47H2O晶体的操作为蒸发浓缩、冷却结晶、______、洗涤、干燥。
【答案】NaOH 使Cu2+和Fe2+完全沉淀 漏斗 烧杯 玻璃棒 Fe Fe+ Cu2+= Fe2++ Cu Fe和Cu,H2SO4,Fe+ 2H+= Fe2++ H2 过滤
【解析】
先加过量的碱,过滤得到氢氧化铜和氢氧化亚铁沉淀,滤液为硫酸钠和氢氧化钠,在沉淀中加入过量的硫酸,溶液C的成分为硫酸铜和硫酸亚铁和硫酸。在溶液中加入过量的铁,过滤出铁和铜,滤液D为硫酸亚铁,在固体E中加入过量的稀硫酸,过滤出铜,实现了回收铜。滤液为硫酸亚铁和硫酸,最后溶液合一起,进行蒸发浓缩,冷却结晶,过滤,得到硫酸亚铁晶体。回收硫酸亚铁。
(1)工业废水中含有硫酸铜和硫酸亚铁,加入 NaOH溶液,使Cu2+和Fe2+完全沉淀,转化为沉淀分离出来。
(2) 操作a的名称为过滤、洗涤,使用的仪器有:漏斗、烧杯、玻璃棒;
(3)加入的试剂为Fe,铁和硫酸铜反应生成硫酸亚铁和铜,用于回收铜,离子方程式为:Fe+ Cu2+= Fe2++ Cu;
(4)固体E为Fe和Cu,加入的试剂④为H2SO4,铁和硫酸反应生成硫酸亚铁和氢气,离子方程式为:Fe+ 2H+= Fe2++ H2↑;
(5)从溶液D和溶液G中得到硫酸亚铁晶体的操作为蒸发浓度、冷却结晶、过滤、洗涤、干燥。


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g)。2 min后该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol/L。下列判断错误的是( )
xC(g)+2D(g)。2 min后该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol/L。下列判断错误的是( )
A. x=1 B. 2 min内A的反应速率为0.3 mol·L-1·min-1
C. B的转化率为40% D. 若混合气体的密度不变则表明该反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂排放的污水中含有FeSO4、CuSO4两种物质。甲、乙、丙三位学生分别设计了从该污水中回收纯净金属铜的方案(如图所示)。

(1)甲、乙、丙提出的实验方案能否得到纯净的金属铜?
甲___,乙___,丙___。(填“能”或“不能”)
(2)在丙同学进行的“酸溶”操作中,加入的酸是___(填“稀盐酸”或“稀硫酸“)。合并的滤液中的主要溶质是___。
(3)丙同学的方案中,过程①加入过量的铁粉时发生反应的化学方程式为___。
(4)操作一、二、三的名称是___,该操作中需使用的玻璃仪器有___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素。A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子。
(1)基态的F3+核外电子排布式是____________________________________________。
(2)B的气态氢化物在水中的溶解度远大于A、C的气态氢化物,原因是______________。
(3)化合物FD3是棕色固体、易潮解、100 ℃左右时升华,它的晶体类型是______________;化合物ECAB中的阴离子与AC2互为等电子体,该阴离子的电子式是____________________。
(4)FD3与ECAB溶液混合,得到含多种配合物的血红色溶液,其中配位数为5的配合物的化学式是______________________________________________________________。
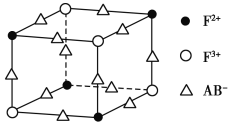
(5)化合物EF[F(AB)6]是一种蓝色晶体,下图表示其晶胞的![]() (E+未画出)。该蓝色晶体的一个晶胞中E+的个数为________。
(E+未画出)。该蓝色晶体的一个晶胞中E+的个数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确且能达到相应实验目的的是
选项 | 实验目的 | 实验操作 |
A | 配制FeCl3溶液 | 将FeCl3固体溶解于适量蒸馏水 |
B | 称取2.0gNaOH 固体 | 先在托盘上各放一张滤纸,然后在右盘上添加2g 砝码,左盘上添加NaOH 固体 |
C | 检验溶液中是否含有NH4+ | 取少最试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
D | 验证铁的吸氧腐蚀 | 将铁钉放入试管中,用盐酸浸没 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.从1L1mol/L的氯化钠溶液中取出10mL,其浓度仍是1mol/L
B.制成0.5L10mol/L的盐酸,需要氯化氢气体112L(标准状况)
C.0.5L2mol/L的氯化钡溶液中,钡离子和氯离子总数为3×6.02×1023
D.10g98%硫酸(密度为1.84g/cm3)与10mL18.4mol/L硫酸的浓度是不同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的表达正确的是( )
A. NH4++H2O=NH3·H2O+H+
B. Na2SO3+2H2O![]() 2NaOH+2H2SO3
2NaOH+2H2SO3
C. BaSO4(s)![]() Ba2+(aq)+SO42-(aq)
Ba2+(aq)+SO42-(aq)
D. NaHCO3=Na++H++CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要450mL 1mol/L的硫酸,现用密度为1.84g/㎝3,溶质的质量分数98%的浓硫酸来配制,有关说法正确的是(设NA阿伏加德罗常数的值)
A. 配制溶液时需的仪器只需要500mL容量瓶、烧杯、玻璃棒、量筒
B. 配制溶液定容时,仰视读数会使溶液的实际浓度偏大
C. 65克单质锌与一定量的该浓硫酸完全反应,生成的气体质量可能为32克
D. 配制该溶液所需浓硫酸体积为24mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一瓶无色澄清的溶液,溶质由NH4NO3、KCl、CuCl2、Ba(NO3)2、Na2CO3中的一种或几种配制而成。为了确定其中的溶质,用该溶液做如下实验:
①取少许溶液,加入足量的盐酸有气泡产生
②再向①的溶液中滴加硝酸银溶液有白色沉淀生成
③取原溶液少量,加入NaOH溶液并加热,产生刺激性气味的气体,并用湿润的红色石蕊试纸检验气体,试纸变蓝
(1)根据以上事实判断:肯定存在的溶质是___;肯定不存在的溶质是___;不能确定是否存在的溶质是___;设计实验证明是否存在该溶质:___。
(2)写出上述实验③中产生刺激性气味气体的反应的化学方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com