
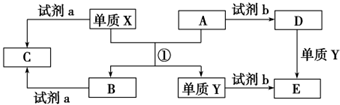
分析 X、Y是生活中用途广泛的两种金属单质,A、B是氧化物,X与A反应得到B与Y,A为红棕色固体,则A为Fe2O3,X与A的反应为铝热反应,则X为Al、Y为Fe、B为Al2O3,试剂a为NaOH溶液时,C为NaAlO2;试剂b为硫酸时,D为硫酸铁、E为硫酸亚铁,据此解答.
解答 解:X、Y是生活中用途广泛的两种金属单质,A、B是氧化物,X与A反应得到B与Y,A为红棕色固体,则A为Fe2O3,X与A的反应为铝热反应,则X为Al、Y为Fe、B为Al2O3,试剂a为NaOH溶液时,C为NaAlO2;试剂b为硫酸时,D为硫酸铁、E为硫酸亚铁.
(1)反应①的化学方程式:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,故答案为:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3;
(2)由D到E的离子方程式:Fe+2Fe3+=3 Fe2+,故答案为:Fe+2Fe3+=3 Fe2+;
(3)若试剂a是NaOH溶液,单质Al与NaOH溶液反应的离子方程式:2Al+2H2O+2OH-═2AlO2-+3H2↑,
故答案为:2Al+2H2O+2OH-═2AlO2-+3H2↑;
(4)若试剂b是H2SO4,工业上用FeSO4、H2SO4和NaNO2为原料制取高效净水剂Fe(OH)SO4,已知还原产物为NO,则该反应的化学方程式是:2FeSO4+H2SO4+2NaNO2=2Fe(OH)SO4+Na2SO4+2NO↑,
故答案为:2FeSO4+H2SO4+2NaNO2=2Fe(OH)SO4+Na2SO4+2NO↑;
(5)工业上电解熔融的Al2O3制取Al时,若阳极产生的气体为氧气,氧气物质的量为$\frac{33.6L}{22.4L/mol}$=1.5mol,根据电子转移守恒可知阴极生成Al为$\frac{1.5mol×4}{3}$=2mol,则阴极产物的质量为2mol×27g/mol=54g,
故答案为:54g.
点评 本题考查无机物的推断,涉及Fe、Al元素单质化合物的性质,注意对铝热反应的掌握,在推断中经常涉及,难度中等.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:解答题
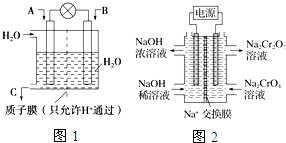 SO2、CO、CO2、NOx是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径.
SO2、CO、CO2、NOx是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑥⑦ | B. | ②④⑥⑦ | C. | ④⑤⑥ | D. | ①③④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Q>W>Z>Y | |
| B. | 元素Y、Q的气态氢化物稳定性:Q>Y | |
| C. | 元素Z、W、Q的最高价氧化物对应水化物相互间能发生反应 | |
| D. | Y与X、Y与Z形成的化合物化学键类型相同. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
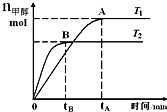 在恒容密闭的容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )
在恒容密闭的容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )| A. | 处于A点的反应体系从T1变到T2,达到平衡时$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$增大 | |
| B. | CO合成甲醇的反应为吸热反应 | |
| C. | 该反应在T1时的平衡常数比T2时的小 | |
| D. | 该反应平衡常数可表示为K=$\frac{c(C{H}_{3}OH)}{c(CO)c({H}_{2})}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 与足量的澄清石灰水反应的现象不同 | |
| B. | 通入BaCl 2溶液时现象相同 | |
| C. | 通入Ba(NO3)₂溶液时现象相同 | |
| D. | 通入石蕊溶液时现象相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇(CH3OH)是一种重要的化工原料,也是一种比较理想的燃料.甲醇在各个领域有着广泛的应用.
甲醇(CH3OH)是一种重要的化工原料,也是一种比较理想的燃料.甲醇在各个领域有着广泛的应用.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com