
��7�֣�(1)���������ھ�������������ˮ������������ҵ�������ΪƯ����
�ٳ������������������ҿ������������е��ʷ�Ӧ���磺
6Ag(s)+O3(g)===3Ag2O(s)����H = -235.8 kJ/mol;
��֪��2 Ag2O(s)===4Ag(s)+O2(g)����H = +62.2kJ/mol;
��Ӧ 2O3��g��= 3O2 ��g�� �ġ�H = kJ/mol��
�ڿ�ѧ��P��Tatapudi��������ʹ�������������µ��ˮ�ķ����Ƶó�����������������Χ��ˮ�в�
�����������������������ɹ������⣬�����缫��ӦʽΪ ��
 ��2���û���̿��ԭ��������������йط�ӦΪ��C(s)+2NO(g) N2(g)+CO2(g) ij�о�С����ij�ܱյ��������(��������������䣬��������������Բ���)�м���NO�������Ļ���̿������(T1��) �����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
��2���û���̿��ԭ��������������йط�ӦΪ��C(s)+2NO(g) N2(g)+CO2(g) ij�о�С����ij�ܱյ��������(��������������䣬��������������Բ���)�м���NO�������Ļ���̿������(T1��) �����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�

����10 min��20 min��ʱ����ڣ���CO2��ʾ�ķ�Ӧ����Ϊ ��
��д���÷�Ӧ��ƽ�ⳣ���ı���ʽK= ��
�����и�������Ϊ�жϸ÷�Ӧ�ﵽƽ��״̬���� (�������ĸ)��
A��������ѹǿ���ֲ��� B��2v��(NO)=v��(N2)
C��������CO2������������� D�����������ܶȱ��ֲ���
��30 minʱ�ı�ijһ��������Ӧ���´ﵽƽ�⣬��ı������������ ��
��һ���¶��£�����NO����ʼŨ��������NO��ƽ��ת���� (����������䡱��С��)��
��7�֣�����1����-285kJ/mol��
��3O2+6H++6e-=3H2O2��
��2������1����0.009/mol/��L.min��
��0.56��
��C��D
�ܼ�СCO2Ũ��
�� ���䡣
��������
�����������1���٢�6Ag��s��+O3��g���T3Ag2O��s������H=-235.8kJ?mol-1��
��2Ag2O��s���T4Ag��s��+O2��g������H=+62.2kJ?mol-1�����ݸ�˹���ɿ�֪�١�2+
�ڡ�3�ɵõ���2O3��g��=3O2��g������Ӧ�ȡ�H=��-235.8kJ?mol-1����2+��+62.2kJ?mol-1��
��3=-285kJ/mol��
�����������µ��ˮ�ķ����Ƶó�����������������Χ��ˮ�в�������缫��ӦʽΪ3H2O-6e-=O3��+6H+�����������������õ������ɹ������⣬��缫��ӦʽΪ3O2+6H++6e-=3H2O2��
��2������10 min��20 min��ʱ����ڣ�CO2��Ũ������0.09mol/L,������CO2��ʾ�ķ�Ӧ����Ϊ0.09mol/L/10min=0.009/mol/��L.min����
�ڷ�Ӧ���е�20minʱ��ƽ��״̬����ʱNO��N2��CO2��ƽ��Ũ�ȷֱ���0.4mol/L��0.3mol/L��
0.3mol/L������ƽ�ⳣ��K=0.32mol/L/0.42mol/L=0.5625��
��A���÷�Ӧ�Ƿ�Ӧǰ������ѹǿ����ķ�Ӧ������ѹǿ���䲻���жϷ�Ӧ�Ƿ��ƽ��״̬������B��ƽ��ʱ��v��(NO)=2v��(N2)������C����Ӧ��ʼʱ������̼���������һֱ����ƽ��״̬ʱ������CO2������������䣬��ȷ��D���÷�Ӧ�й�����룬�������������һֱ��������������䣬����������ܶ�һֱ�ڱ䣬����ƽ��ʱ�������ܶȲ��ٱ仯����ȷ����ѡCD��
�ܴӱ������ݿ�֪��40minʱNO��Ũ�ȼ�С��������Ũ����������̼��Ũ�ȼ�С�������ж�ƽ�������ƶ����ı�������Ǽ�С������̼��Ũ�ȣ�ʹƽ�������ƶ���
�ݸ÷�Ӧ�Ƿ�Ӧǰ����������ʵ�������ķ�Ӧ���ı�NO��Ũ�ȴﵽ��ƽ���ǵ�Чƽ�⣬����NO��ת���ʲ��䡣
���㣺�����˹���ɵ�Ӧ�ã��绯ѧԭ����Ӧ�ã���ѧƽ�����۵�Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ������ҵˮƽ������Ӧ�Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�У�������ȡ����Ӧ�������
A��CH4+Cl2  CH3Cl+HCl
CH3Cl+HCl
B��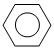 +HNO3
+HNO3 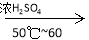
 +H2O
+H2O
C��2CH3CH2OH+O2 2CH3CHO+2H2O
2CH3CHO+2H2O
D��CH3COOCH2CH3+H2O  CH3COOH+CH3CH2OH
CH3COOH+CH3CH2OH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��9�֣���2 L�ܱ������ڣ�800��ʱ��Ӧ2SO2(g)��O2(g) 2SO3(g)��ϵ�У�n(SO2)��ʱ��ı仯���±���
2SO3(g)��ϵ�У�n(SO2)��ʱ��ı仯���±���
ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)(mol) | 0.020 | 0. 010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)������Ӧ________(��ǡ����ǡ�)���淴Ӧ���ڵ� 5 sʱ��SO2��ת����Ϊ________��
(2)��ͼ��ʾ����ʾSO3�仯���ߵ���_____����O2��ʾ��0 s��2 s�ڸ÷�Ӧ��ƽ�����ʣ�v��__��
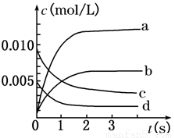
(3)��˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
a��v(SO3)��2v(O2)���� b�����������SO2������������ֲ���
c��v��(SO2)��2v��(O2) d���������ܶȱ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ڿ��淴ӦA(g)��3B(s) 2C(g)��2D(g)���ڲ�ͬ�����µĻ�ѧ��Ӧ���ʣ����з�Ӧ���������� (����)
2C(g)��2D(g)���ڲ�ͬ�����µĻ�ѧ��Ӧ���ʣ����з�Ӧ���������� (����)
A��v(A)��0.5 mol��L��1��min��1 B��v(B)��1.2 mol��L��1��s��1
C��v(D)��0.4 mol��L��1��min��1 D��v(C)��0.1 mol��L��1��s��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ�����и߶��꼶��ѧ�������ģ�����ѧ�Ծ��������棩 ���ͣ�������
��6�֣���50mL a mol��L-1��������Һ�У�����6.4g Cu��ȫ���ܽ⣬��������Ļ�ԭ����ֻ��NO2��NO������Ӧ����Һ������ˮϡ����100mLʱ���c(NO3-)=3 mol��L-1��
��1����ϡ�ͺ����Һ��pH= ��
��2����a=9�������ɵ�������NO2�����ʵ���Ϊ mol��
��3����������������Ⱦ�ķ���֮һ����NaOH��Һ�������գ���Ӧԭ�����£�
NO2+NO+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO2+NaNO3+H2O
����������NO2��NO�Ļ������ͨ��1mol��L-1��NaOHǡ�ñ����գ���NaOH��Һ�����Ϊ mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ�����и߶��꼶��ѧ�������ģ�����ѧ�Ծ��������棩 ���ͣ�ѡ����
�Ե������Ǵӷ仨��ֲ������ȡ�õ����������ʣ���ṹ ��ͼ������������ȷ����
��ͼ������������ȷ����

A���Ե��������ڷ�����
B��1mol�Ե���������ܺ�9mol���������ӳɷ�Ӧ
C���Ե�������Է���ˮ�ⷴӦ��ȡ����Ӧ��������Ӧ
D��lmol�Ե���������ܺͺ�5mol NaOH��ˮ��Һ��ȫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ�����и߶��꼶��ѧ�������ģ�����ѧ�Ծ��������棩 ���ͣ�ѡ����
һ�������£����ܱպ��������м���1.0 mol��L-1X��������Ӧ��2X(g)  Y(g)+Z(g) ��H��0����Ӧ��8minʱ�ﵽƽ�⣻��14minʱ�ı���ϵ���¶ȣ� 16minʱ������ƽ�⡣X�����ʵ���Ũ�ȱ仯��ͼ��ʾ�������й�˵����ȷ����
Y(g)+Z(g) ��H��0����Ӧ��8minʱ�ﵽƽ�⣻��14minʱ�ı���ϵ���¶ȣ� 16minʱ������ƽ�⡣X�����ʵ���Ũ�ȱ仯��ͼ��ʾ�������й�˵����ȷ����
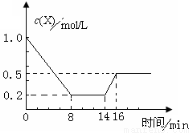
A��0��8min��Y��ʾ�÷�Ӧ����Ϊ0.1mol��L-1��min��1
B��8minʱ�ﵽƽ�⣬�÷�Ӧ��ƽ�ⳣ��ΪK= 0.5
C��14minʱ���ı�ķ�Ӧ���ǽ������¶�
D��16minʱ������Ӧ���ʱ�8minʱ������Ӧ���ʴ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ�����߿�ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��Һ�к��е����ӿ�����K+��Ba2+��A13+��Mg2+��AlO2����CO32����SiO32����Cl���еļ��֣��ֽ�������ʵ�飺
��ȡ������Һ������������Һ��������������
����ȡ����ԭ��Һ����μ���5mL 0.2mol��L-1���ᣬ�����������ǣ���ʼ���������������࣬���������������������壬��������������ʧ��
���������ڳ�����ʧ�����Һ�У��ټ�����������������Һ�ɵõ�����0.43g��
����˵������ȷ����
A������Һ��һ������Ba2+��Mg2+��A13+��SiO32����Cl��
B������Һ��һ������K+��AlO2����CO32����Cl��
C������Һ�Ƿ���K+������ɫ��Ӧ������ɫ�ܲ���Ƭ��
D�����ܺ���Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ����������ͨ��30 mLŨ��Ϊ10.00 mol/L����������Ũ��Һ�У���������ʱ�����Һ���γ�NaCl��NaClO��NaClO3������ϵ�������жϲ���ȷ����
A����NaOH��Ӧ������һ��Ϊ0.15 mol
B��n(Na��)��n(Cl��) ����Ϊ7��3
C������Ӧ��ת�Ƶĵ���Ϊn mol����nһ������0.15 mol
D��n(NaCl)��n(NaClO)��n(NaClO3)����Ϊ7��2��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com