
| A”¢¼ÓČėĀČ»Æ±µČÜŅŗÓŠ°×É«³ĮµķÉś³É£¬ŌŁ¼ÓĻ”ŃĪĖį£¬³Įµķ²»ĻūŹ§£¬Ņ»¶ØÓŠSO42- |
| B”¢Na2O2ÓėCO2·“Ó¦£¬Na2O2ŹĒŃõ»Æ¼Į”¢CO2ŹĒ»¹Ō¼Į |
| C”¢ĻņŠĀÖʵÄFeSO4ČÜŅŗÖŠµĪČėŹŹĮæµÄNaOHČÜŅŗ£¬·ÅÖĆʬæĢ£¬Õūøö·“Ó¦¹ż³ĢµÄŃÕÉ«±ä»ÆŹĒ£ŗĒ³ĀĢÉ«ČÜŅŗ”ś°×É«³Įµķ”ś»ŅĀĢÉ«³Įµķ”śŗģŗÖÉ«³Įµķ |
| D”¢³ĘČ”µČÖŹĮæµÄĮ½·ŻĀĮ·Ū£¬·Ö±š¼ÓČė¹żĮæµÄĻ”ŃĪĖįŗĶ¹żĮæµÄNaOHČÜŅŗ£¬Ōņ·Å³öĒāĘųµÄĢå»ż£ØĶ¬ĪĀĶ¬Ń¹ĻĀ£©²»ĻąµČ |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ÖŠŗĶČČµÄ²ā¶ØŹµŃéµÄ¹Ų¼üŹĒ ŅŖ±Č½Ļ×¼Č·µŲÅäÖĘŅ»¶ØµÄĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗ£¬ŌŚŹµŃé¹ż³ĢÖŠŅŖ¾”Įæ±ÜĆāČČĮæµÄÉ¢Ź§£¬ŅŖĒó±Č½Ļ×¼Č·µŲ²āĮæ³ö·“Ó¦Ē°ŗóČÜŅŗĪĀ¶ČµÄ±ä»Æ£®»Ų“šĻĀĮŠĪŹĢā£ŗ
ÖŠŗĶČČµÄ²ā¶ØŹµŃéµÄ¹Ų¼üŹĒ ŅŖ±Č½Ļ×¼Č·µŲÅäÖĘŅ»¶ØµÄĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗ£¬ŌŚŹµŃé¹ż³ĢÖŠŅŖ¾”Įæ±ÜĆāČČĮæµÄÉ¢Ź§£¬ŅŖĒó±Č½Ļ×¼Č·µŲ²āĮæ³ö·“Ó¦Ē°ŗóČÜŅŗĪĀ¶ČµÄ±ä»Æ£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢¶¬ĢģŹ³ĪļÄŃŅŌøÆ°Ü |
| B”¢ÓĆ¹żĮæO2ÓėSO2»ģŗĻÖĘSO3 |
| C”¢½«Ź¢NO2µÄĘæ×Ó·ÅČė±łĖ®ÖŠ£¬ŃÕÉ«±äĒ³ |
| D”¢¹¤ŅµÉĻÖĘNH3Ź±²śÓĆøßŃ¹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢Ä³ČÜŅŗÖŠ¼ÓĻõĖįŅųČÜŅŗÉś³É°×É«³Įµķ£¬ĖµĆ÷ŌČÜŅŗÖŠÓŠCl- |
| B”¢Ä³ČÜŅŗÖŠ¼ÓBaCl2ČÜŅŗÉś³É°×É«³Įµķ£¬ĖµĆ÷ŌČÜŅŗÖŠÓŠSO42- |
| C”¢Ä³ČÜŅŗÖŠ¼ÓNaOHČÜŅŗÉś³ÉĄ¶É«³Įµķ£¬ĖµĆ÷ŌČÜŅŗÖŠÓŠCu2+ |
| D”¢Ä³ČÜŅŗ¼ÓĻ”ĮņĖįÉś³É°×É«³Įµķ£¬ĖµĆ÷ŌČÜŅŗÖŠÓŠBa2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| AӢAl3+ӢSO42-ӢNH4+ӢCl- |
| BӢK+ӢFe2+ӢCl-ӢNO3- |
| CӢK+ӢNa+ӢCl-ӢSO42- |
| DӢNa+ӢK+ӢNO3-ӢHCO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
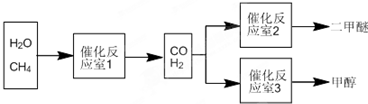
| ĪļÖŹ | CH3OH | CH3OCH3 | H2O |
| ÅضČ/£Ømol?L-1£© | 0.44 | 0.6 | 0.6 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com