
| A、若维持温度不变,起始时②中投人3mol A、1 mol B;③中投入3 mol A、l mol B和2mol C,则达到平衡时,两容器中B的转化率②=③ |
| B、若起始温度相同,分别向三个容器中充入3 mol A和1mol B,则达到平衡时各容器中C物质的百分含量由大到小的顺序为③>②>① |
| C、若起始温度相同,分别向三个容器中充入1 mol A和1molB则达到平衡时各容器中C物质的百分含量一定相同 |
| D、若起始温度相同,分别向三个容器中充入3a mol A和a molB则达到平衡时各容器中A物质的转化率一定相同 |


科目:高中化学 来源: 题型:
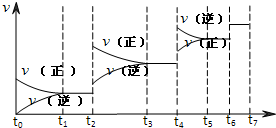 可逆反应C(s)+H2O(g)?H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率v与时间t的关系如图.
可逆反应C(s)+H2O(g)?H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率v与时间t的关系如图.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Zn2++2OH-═Zn(OH)2↓ ZnCO3+2NaOH═Zn(OH)2↓+Na2CO3 |
| B、Ba2++SO42-═BaSO4 Ba(OH)2+H2SO4═BaSO4↓+2H2O |
| C、Ag++Cl-═AgCl↓ AgNO3+KCl═AgCl↓+KNO3 |
| D、Cu+2Ag+═Cu2++2Ag Cu+2AgCl═CuCl2+2Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:
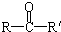 (R、R′代表烷基或H原子)发生缩合反应生成新的有机物和水.
(R、R′代表烷基或H原子)发生缩合反应生成新的有机物和水.
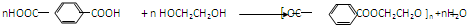
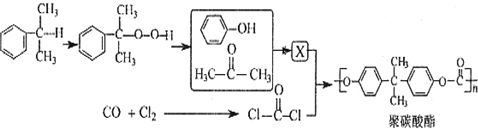
 反应合成聚碳酸酯的化学方程式(不必写反应条件):
反应合成聚碳酸酯的化学方程式(不必写反应条件):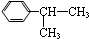 互为同分异构体的有机物有
互为同分异构体的有机物有查看答案和解析>>
科目:高中化学 来源: 题型:
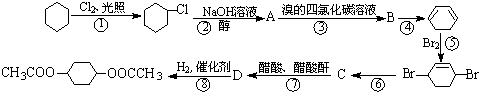
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等体积等物质的量浓度的NaClO溶液与NaCl(aq) 溶液中离子总数大小:N后>N前 |
| B、常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH) |
| C、0.1 mol?L-1Na2CO3溶液与0.1 mol?L-1NaHCO3溶液等体积混合c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) |
| D、硫酸氢铵溶液中滴加氢氧化钠至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(C8H10)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n(C8H8)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com