索尔维制碱法距今已有140多年的历史,为当时世界各国所采用,后被中国的侯氏制碱法取代.索尔维法的生产流程如下所示:
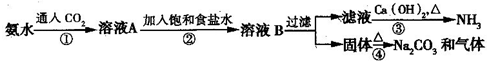
索尔维法能实现连续生产,但食盐的利用率只有70%,且副产品CaCl
2没有合适的用途,会污染环境.
1940年我国化学家侯德榜先生经过多次试验,弥补了索尔维法的技术缺陷,加以改进,食盐利用率高达96%,得到了纯碱和氯化铵两种产品,被称为“侯氏制碱法”.此方法的基本原理如下:
①向30~50℃的饱和食盐水中,先通入氨气至饱和,再通入CO
2,从而得到碳酸氢钠沉淀.
②过滤,将滤渣加热而得产品.
③向滤液中加入细食盐末,调节温度为10~15℃,使NH
4Cl沉淀,过滤,滤渣为NH
4Cl产品,滤液为饱和食盐水.
请回答下列问题:
(1)写出向含氨气的饱和NaCl溶液中通入CO
2 时发生反应的两个化学方程式:
CO2+NH3+H2O=NH4HCO3、NH4HCO3+NaCl=NaHCO3↓+NH4Cl
CO2+NH3+H2O=NH4HCO3、NH4HCO3+NaCl=NaHCO3↓+NH4Cl
.
(2)不能向饱和NaCl溶液中通入CO
2 制NaHCO
3的原因是
H2CO3酸性比盐酸弱,CO2与NaCl不反应
H2CO3酸性比盐酸弱,CO2与NaCl不反应
;也不能采用先向饱和NaCl溶液中通入CO
2,再通入NH
3的方法制NaHC0
3 的原因是
CO2在NaCl溶液中溶解度较小,生成NaHCO3太少不会结晶析出
CO2在NaCl溶液中溶解度较小,生成NaHCO3太少不会结晶析出
.
(3)写出在索尔维法生产过程中,生成CaCl
2 的化学反应方程式为
2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O
2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O
.
(4)在侯氏制碱法中,
二氧化碳和饱和食盐水
二氧化碳和饱和食盐水
(填物质名称)可以循环利用.
(5)侯氏制碱法与索尔维法相比,其优点是
使NH4Cl析出,可做氮肥;减少无用的CaCl2生成,原料NaCl充分利用
使NH4Cl析出,可做氮肥;减少无用的CaCl2生成,原料NaCl充分利用
(任写一条即可).

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案