
 X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )| A. | Z的氧化物对应的水化物一定是一种强酸 | |
| B. | 原子半径大小顺序是X>Y>Z | |
| C. | Y的单质比Z的单质更易与氢气反应 | |
| D. | Z的单质与Fe反应形成的化合物中,铁元素显+3价 |
分析 根据Y原子的最外层电子数是次外层电子数的3倍可知,Y为氧元素,根据位置关系推出X为N,Z为S,W为Cl.
A.二氧化硫对应的酸为亚硫酸属于弱酸;
B.同一周期,从左到右,原子半径逐渐减小,电子层数越多半径越大;
C.元素的非金属性越强,对应的单质与氢气化合更容易;
D.S的单质具有弱氧化性,与变价金属反应生成低价产物.
解答 解:A.Z为S元素,其氧化物由二氧化硫和三氧化硫,二氧化硫对应的酸为亚硫酸属于弱酸,故A错误;
B.同一周期,从左到右,原子半径逐渐减小,故X>Y,Z在下一周期,则原子半径:Z>X>Y,故B错误;
C.元素的非金属性越强,对应的单质与氢气化合更容易,非金属性:O>S,则O的单质比S的单质更易与氢气反应,故C正确;
D.S的单质与Fe反应形成的化合物中,铁元素显+2价,故D错误.
故选C.
点评 本题考查了元素周期律中位、构、性三者之间的关系,元素的推断是解答的关键,注意原子结构中的关系及非金属性的比较,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 明矾[KAl(SO4)2•12H2O]溶于水会形成胶体,因此可用于自来水的杀菌消毒 | |
| B. | 小苏打是制作面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 | |
| C. | 蛋白质、淀粉、油脂等都能在人体内水解并提供能量 | |
| D. | 纯净的二氧化硅是现代光学及光纤制品的基本原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
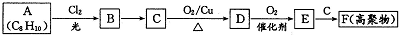
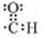 ;E一→F反应类型为缩聚反应.
;E一→F反应类型为缩聚反应. .
.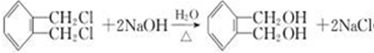 .
.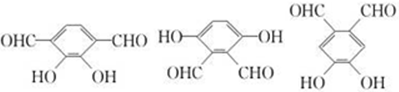 (2种即可).
(2种即可).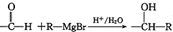 现发生反应D+G$\stackrel{H+/H_{2}O}{→}$H$→_{△}^{浓H_{2}SO_{4}}$J(
现发生反应D+G$\stackrel{H+/H_{2}O}{→}$H$→_{△}^{浓H_{2}SO_{4}}$J( ),则
),则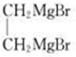 ,
,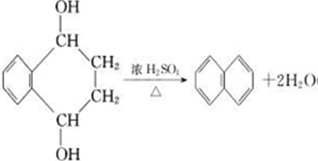 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氨水吸收过量的二氧化硫:NH3•H2O+SO2=NH4++HSO3- | |
| B. | 在澄清石灰水中通入少量二氧化碳:OH-+CO2=HCO3- | |
| C. | 向溴化亚铁中通入少量氯气:2Br-+Cl2=2Cl-+Br2 | |
| D. | 用氢氧化钠吸收多余的氯气:OH-+Cl2=2Cl-+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 结构或性质信息 |
| X | 其原子最外层电子数是内层电子数的2倍 |
| Y | 基态原子最外层电子排布为nsnnpn+1 |
| Z | 非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰 |
| M | 单质在常温、常压下是气体.基态原子的M层上有1个未成对的p电子 |
| Q | 其与X形成的合金为目前用量最多的金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

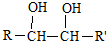 $\stackrel{HIO_{4}}{→}$RCHO+R′CHO
$\stackrel{HIO_{4}}{→}$RCHO+R′CHO . B→H的反应类型是取代反应.
. B→H的反应类型是取代反应.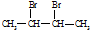 +2NaOH
+2NaOH CH3-C≡C-CH3+2NaBr+2H2O.
CH3-C≡C-CH3+2NaBr+2H2O.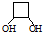 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有A、B、C、B、D、E五种元素,B原子得到一个电子后3P轨道全充满,A+比B形成的简单离子少一个电子层,C原子的P轨道半充满,它形成的氢化物的沸点是同主族元素的氢化物中最低的,D和E是位于同一主族的短周期元素,E元素的最高化合价与最低化合价的代数和为零,E在其最高价氧化物中的质量分数为46.67%.请回答:
有A、B、C、B、D、E五种元素,B原子得到一个电子后3P轨道全充满,A+比B形成的简单离子少一个电子层,C原子的P轨道半充满,它形成的氢化物的沸点是同主族元素的氢化物中最低的,D和E是位于同一主族的短周期元素,E元素的最高化合价与最低化合价的代数和为零,E在其最高价氧化物中的质量分数为46.67%.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com