
| A. | 步骤①、③的操作分别是过滤、萃取分液 | |
| B. | 可用淀粉溶液检验步骤②的反应是否进行完全 | |
| C. | 步骤③中加入的有机溶剂是乙醇 | |
| D. | 步骤④的操作是过滤 |
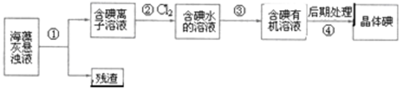
分析 实验室从海带中提取碘:海带灼烧成灰,浸泡溶解得到海带灰悬浊液,通过①过滤,得到不溶的残渣,滤液为含碘离子的溶液,加入氧化剂②Cl2,将碘离子氧化成碘单质,利用有机溶剂萃取出碘单质③,再通过蒸馏④提取出碘单质.
A.淀粉能检验碘单质不能检验碘离子;
B.萃取剂不能和溶质反应,且萃取剂和原溶剂不能互溶;
C.碘易溶于有机溶剂,应该用蒸馏的方法提取碘;
D.难溶性固体和溶液采用过滤的方法分离;同一溶质在不同溶剂中的溶解度不同的溶质可以采用萃取的方法分离.
解答 解:A.步骤①分离固体和液体用过滤,③将碘水中的碘单质分离出来,选择合适的萃取剂进行萃取即可,故A正确;
B.碘遇淀粉试液变蓝色,淀粉能检验碘单质不能检验碘离子,故B错误;
C.萃取剂和原溶剂不能互溶,酒精和水互溶,所以不能作萃取剂,故C错误;
D.碘易溶于有机溶剂,所以不能过滤,步骤④应该用蒸馏的方法提取碘,故D错误;
故选A.
点评 本题以实验室从海藻里提取碘为载体考查了混合物分离的方法、碘的性质、萃取剂的选取等知识点,明确物质分离提纯的选取方法、萃取剂的选取标准、每一步发生的反应是解答关键,题目难度不大,注意常用混合物分离的方法.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 醋酸 | HD |
| B | 冰醋酸 | 汽油 | 苛性钾 | 碳酸氢钠 | 乙醇 |
| C | 烧碱 | 蔗糖溶液 | 氯化钠 | 氨水 | 三氧化硫 |
| D | 胆矾 | 石灰水 | 硫酸钡 | H2O | NH3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物熔沸点较高、共价化合物熔沸点较低 | |
| B. | 非金属原子间不可能形成离子化合物 | |
| C. | 确定某化合物为离子化合物,可以用融化时能否导电来判断 | |
| D. | 共价化合物中可能有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
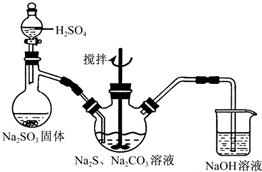 硫代硫酸钠(Na2S2O3)俗称海波,可用于纸浆漂白作脱氯剂等.实验室通过如下反应制取:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2.
硫代硫酸钠(Na2S2O3)俗称海波,可用于纸浆漂白作脱氯剂等.实验室通过如下反应制取:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
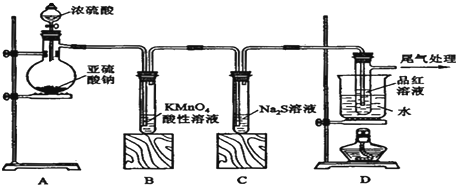
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 实验室采购了部分化学药品.如图是从化学试剂商店买回的硫酸试剂标签上的部分内容.下列说法正确的是( )
实验室采购了部分化学药品.如图是从化学试剂商店买回的硫酸试剂标签上的部分内容.下列说法正确的是( )| A. | 该硫酸的物质的量浓度为9.2mol•L-1 | |
| B. | 1molAl与足量的该硫酸反应产生3g氢气 | |
| C. | “化学纯”是指这种硫酸只含H2SO4和H2O分子 | |
| D. | 配制460mL2.3mol•L-1的稀硫酸需量取该硫酸62.5 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
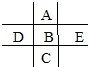 如图为周期表前四周期的一小部分,A、B、C、D、E的位置关系如图所示.其中B元素的最高价是负价绝对值的3倍,它的最高氧化物中含氧60%,回答下列问题:
如图为周期表前四周期的一小部分,A、B、C、D、E的位置关系如图所示.其中B元素的最高价是负价绝对值的3倍,它的最高氧化物中含氧60%,回答下列问题: .A单质的电子式为
.A单质的电子式为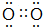 .
.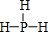 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com