
| A. | 能量守恒原理 | B. | 能量最低原则 | C. | 泡利不相容原理 | D. | 洪特规则 |
分析 能量最低原理:原子核外电子先占有能量低的轨道,然后依次进入能量高的轨道;
泡利不相容原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子;
洪特规则:洪特规则是在等价轨道(相同电子层、电子亚层上的各个轨道)上排布的电子将尽可能分占不同的轨道,且自旋方向相同.
解答 解:P原子2p能级上有3个轨道,2p能级上有2个电子,2个电子应该排在2个不同的轨道上,且自旋方向相同,若将P原子的电子排布式写成1s22s22p${\;}_{x}^{2}$,它违背了洪特规则,正确的电子排布式为:1s22s22px12py1,故选D.
点评 本题考查了原子结构构造原理,明确这几个概念是解本题关键,难度不大.


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 各物质的量浓度之比为c(M):c(N):c(P)=2:2:3 | |
| B. | 平衡混合物体积是反应开始前的$\frac{3}{5}$ | |
| C. | 平衡混合物中各物质的量浓度相等 | |
| D. | 单位时间内,若消耗了 a mol M 物质,则同时也消耗了 1.5a mol P 物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
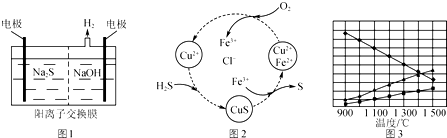
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O+H2O═2NaOH | B. | H2+CuO═Cu+H2O | ||
| C. | CaCO3═CaO+CO2↑ | D. | KOH+HNO3═KNO3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量相同、密度不同的CO与N2所含的原子数目一定相等 | |
| B. | 质量不同、密度相同的CO与N2所含分子数可能相同 | |
| C. | 分子数不同的CO与N2的体积一定不等 | |
| D. | 体积相同的CO与N2的质量一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和滴定实验时,用待测液润洗锥形瓶 | |
| B. | 配制一定物质的量浓度溶液时,在溶解、移液、洗涤、定容时均要用到玻璃棒 | |
| C. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| D. | NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com