
【题目】某盐A是由三种元素组成的化合物,某研究小组按如图流程探究其组成:

请回答:
(1)写出红棕色固体C的化学式________________。
(2)写出A受热分解反应的化学方程式________________。
(3)写出检验A中阳离子的实验方案________________。
【答案】 Fe2O3 2FeSO4=Fe2O3+SO3↑+SO2↑ 取少量试样配成溶液,滴入KSCN溶液,若不变色,再滴加少量氯水,出现血红色,证明有亚铁离子
【解析】本题考查无机物的推断,涉及铁及其化合物的性质,根据框图提供的信息解答。气体能与BaCl2溶液反应,产生2.33g的白色沉淀,则该气体中有SO3,2.33g白色沉淀是BaSO4 ,物质的量为0.01mol,SO3的物质的量为0.01mol,448mL气体B的物质的量为0.02mol,则气体B中还有0.01mol的SO2,红棕色固体与盐酸反应生成黄色溶液,则红棕色固体C为Fe2O3,氧化铁与盐酸反应生成氯化铁和水,氯化铁溶液呈黄色,氧化铁的物质的量为1.6g÷160g/mol= 0.01mol,化合物A中铁和硫元素的物质的量之比为1:1,质量为(56+32)g/mol×0.02mol= 1.76g,盐A是由三种元素组成的化合物,则另一种元素为氧,质量为3.04g-1.76g=1.28g,物质的量为0.08mol,所以化合物A中铁、硫、氧的物质的量之比为1:1:4,A是FeSO4。
(1)根据上述分析,红棕色固体C为氧化铁,化学式为Fe2O3。
(2)根据上述分析,A为FeSO4,受热分解生成氧化铁、SO2和SO3,反应的化学方程式为2FeSO4=Fe2O3+SO3↑+SO2↑ 。
(3)A为FeSO4,根据Fe2+的检验方法,检验FeSO4中Fe2+离子的实验方案是取少量试样配成溶液,滴入KSCN溶液,若不变色,再滴加少量氯水,出现血红色,证明有亚铁离子。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】19世纪中叶,门捷列夫总结了如表所示的元素化学性质的变化情况。请回答:
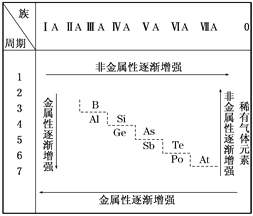
(1)门捷列夫的突出贡献是__________。
A.提出了原子学说
B.提出了分子学说
C.发现了元素周期律
D.发现能量守恒定律
(2)该表变化表明__________。
A.事物的性质总是在不断地发生变化
B.元素周期表中最右上角的氦元素是非金属性最强的元素
C.第ⅠA族元素的金属性肯定比同周期的第ⅡA族元素的金属性强
D.物质发生量变到一定程度必然引起质变
(3)按照表中元素的位置,认真观察从第ⅢA族的硼到第ⅦA族的砹连接的一条折线,我们能从分界线附近找到__________。
A.耐高温材料 B.新型农药材料
C.半导体材料 D.新型催化剂材料
(4)据报道,美国科学家制得一种新原子![]() X,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是__________。
X,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是__________。
A.这种原子的中子数为167 B.它位于元素周期表中第6周期
C.这种元素一定是金属元素 D.这种元素的原子易与氢化合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在科学史上每一次重大的发现都极大地推进了科学的发展。我国宁波藉科学家屠呦呦获得诺贝尔生理学或医学奖,她成为首获科学类诺贝尔奖的中国本土科学家。她获奖的原因是发现了
A. 青蒿素 B. 合成氨的生产工艺
C. 提示了燃烧的本质 D. 维生素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中相邻元素之间原子序数的关系正确的是( )
A.相邻主族的元素的原子序数之差一定都是1
B.主族中相邻元素的原子序数之差只有1、11、25
C.相邻周期元素的原子序数之差一定都是8
D.相邻周期元素的原子序数之差可能有2、8、18、32
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中,一定能大量共存的是( )
A. 无色溶液中:[Al(OH)4]-、K+、OH-、NO![]()
B. 能与铝片反应产生氢气的溶液中:Al3+、Cl-、Fe2+、NO![]()
C. 常温下,pH=2的溶液中:SO![]() 、Cl-、K+、SiO
、Cl-、K+、SiO![]()
D. 含有较多Fe3+的溶液中:Na+、SO![]() 、SCN-、I-
、SCN-、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在pH=13的溶液中,能大量共存的离子组是:
A. Na+、NH4+、Clˉ、SO42ˉ B. K+、Na+、AlO2ˉ、Clˉ
C. Mg2+、K+、NO3ˉ、Clˉ D. K+、Na+、Al3+、SO42ˉ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。

(1)甲中负极的电极反应式为____________。
(2)乙中B极为_____(填“阴极”或“阳极”),该电极上析出的气体在标准状况下的体积为____。
(3)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2,则图中③线表示的是_________________(填离子符号)的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要___________ mL 2. 0 mol/L NaOH溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】截止到2013年12月末,中国光伏发电新增装机容量达到10.66GW,光伏发电累计装机容量达到17.I6GW,图为光伏并网发电装置电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。下列叙述中正确的是

A. N型半导体为正极,P型半导体为负极
B.制氢装置溶液中电子流向:从B极流向A极
C.X2为氧气
D.工作时,A极的电极反应式为CO(NH2) 2+8OH--6e-═CO32-+N2↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知常温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,则该溶液的pH= ,此酸的电离平衡常数K= ,由HA电离出的H+的浓度约为水电离出的H+的浓度的 倍。
(2)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶剂。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
①向该溶液中加入少量盐酸时,发生反应的离子方程式是 ,向其中加入少量KOH溶液时,发生反应的离子方程式是 。
②现将0.04mol﹒L-1HA溶液和0.02mol﹒L-1NaOH溶液等体积混合,得到缓冲溶液。
a、若HA为HCN,该溶液显碱性,则溶液中c(Na+) c(CN-)(填“<”、“=”或“>”)。
b、若HA为CH3COOH,该溶液显酸性,溶液中所有的离子按浓度由大到小排列的顺序是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com