
【题目】下列说法正确的是 ( )
A. 自发反应一定是熵增大,非自发反应一定是熵减小
B. 常温下pH=10碳酸钠的溶液,由水电离出的H+浓度等于1×10-10mol/L
C. 可溶性盐在水中完全电离是强电解质,而难溶性盐在水中只能部分电离
D. 对于反应2X(g)+Y(g)![]() Z(g)ΔH>0,增加X的量,ΔH不变
Z(g)ΔH>0,增加X的量,ΔH不变
【答案】D
【解析】
A项、自发反应不一定是熵增大,如△H<0,△S<0低温下反应自发进行,非自发反应不一定是熵减小或不变,也可以增大,如△H>0,△S>0低温下是非自发进行的反应,故A错误;
B项、常温下pH=10碳酸钠的溶液,因为盐的水解促进了水的电离,即水电离出的c(H+)等于水电离出的c(OH-)等于溶液中的c(OH-),溶液中的c(OH-)=Kw/1×10-10mol/L=1×10-4mol/L,故B错误;
C项、可溶性盐在水中完全电离是强电解质,难溶性盐如碳酸钙难溶于水,但溶解部分完全电离,CaCO3是强电解质,故C错误;
D项、对于反应2X(g)+Y(g)![]() Z(g)ΔH>0,增加X的量,平衡正向移动,吸收的热量增大,但ΔH不变,故D正确。
Z(g)ΔH>0,增加X的量,平衡正向移动,吸收的热量增大,但ΔH不变,故D正确。
故选D。


科目:高中化学 来源: 题型:
【题目】已知1 L Al(NO3)3和Cu(NO3)2的混合溶液中c(NO3-)=0.7mol/L,用石墨作电极电解该混合溶液,当通电一段时回后,两极均有气体生成(电解前后溶液的体积变化忽略不计)。下列说法正确的是
A. 电解后溶液的pH增大 B. 电解过程中在阴极附近有沉淀生成
C. 原混合溶液中c(Al3+)=0.7mol/L D. 电解后溶液中仍有Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,体积一定的密闭容器中进行如下反应:X(g)+Y(g)![]() Z(g)+W(s) ΔH>0,下列叙述不正确的是
Z(g)+W(s) ΔH>0,下列叙述不正确的是
A. 在容器中加入氩气,反应速率不变
B. 加入少量W,逆反应速率不变
C. 升高温度,正反应速率增大,逆反应速率减小
D. 将容器的体积压缩,可增大单位体积内活化分子数,有效碰撞次数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭的2 L容器中装有4 mol SO2和2 mol O2,在一定条件下开始反应。2 min末测得容器中有1.6 mol SO2,请计算:
(1)2 min末SO3的浓度;
(2)2 min内SO2的平均反应速率;
(3)2 min末SO2的转化率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是治疗高血压的药物“比索洛尔”的中间体,一种合成G的路线如下:

已知以下信息:
①A的核磁共振氢谱为单峰;B的核磁共振氢谱为三组峰,峰面积比为6∶1∶1。
②D的苯环上仅有两种不同化学环境的氢;1 mol D可与1 mol NaOH或2 mol Na反应。
回答下列问题:
(1)A的结构简式为____________。
(2)B的化学名称为____________。
(3)C与D反应生成E的化学方程式为_________________。
(4)由E生成F的反应类型为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
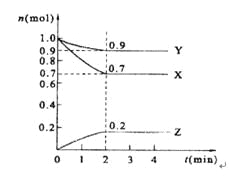
(1)X的转化率是______;
(2)由图中所给数据进行分析,该反应的化学方程式为______;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=__________;
(4)当反应进行到第____min,该反应是达到平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】造纸、炼焦、医药、塑料等行业的废水中常含有苯酚(C6H5OH),会对人类的生产和生活造成极大的危害。含酚废水的处理是环境科学领域的热点问题,下面介绍三项新技术。
电渗析
苯酚具有微弱的酸性,可利用电场促使C6H5O-定向移动、脱离废水,并富集回收。其电离方程式、电渗析装置示意图如下:
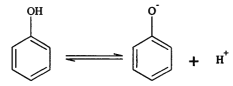
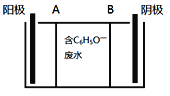
(1)为促进苯酚电离并增强溶液导电能力,可向废水中加入__________。
(2)A、B分别为离子交换膜,其中A应该是______(填“阳”或“阴”)离子交换膜。
催化重整制氢
在固定床反应器中,用含Rh催化剂使苯酚与水蒸气反应转化为氢气和二氧化碳。已知:2H2(g)+ O2(g)== 2H2O(g) ΔH1=-483.6 kJ·mol-1
C6H5OH(g)+ 7O2(g)== 6CO2(g)+ 3H2O(g) ΔH2=-2742.4 kJ·mol-1
(3)那么,反应C6H5OH(g)+ 11H2O(g)== 6CO2(g)+ 14H2(g) ΔH=_________kJ·mol-1。
活性炭纤维(ACF)物理吸附
ACF是一种活性炭纤维,不溶于水,具有多孔结构,可吸附苯酚等多种有机物质。下表是实验室里在不同温度下用0.50 g ACF吸附处理1 L苯酚溶液的相关数据。
T / ℃ | 25 | 35 | 45 | 55 | 65 |
起始苯酚浓度 / mol·L-1 | 1.50×10-3 | 1.50×10-3 | 1.50×10-3 | 1.50×10-3 | 1.50×10-3 |
平衡苯酚浓度 / mol·L-1 | 5.00×10-4 | 6.43×10-4 | 7.85×10-4 | 9.12×10-4 | 1.13×10-3 |
(4)由表格数据可知,C6H5OH(aq) + ACF(s) ![]() C6H5OH·ACF(s,吸附态) ΔH_____0(填“>”或“<”)。
C6H5OH·ACF(s,吸附态) ΔH_____0(填“>”或“<”)。
(span>5)已知:吸附平衡常数KF=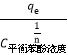 ,(其中,平衡时单位质量吸附剂对苯酚的吸附量
,(其中,平衡时单位质量吸附剂对苯酚的吸附量![]() ;n为与ACF吸附能力相关的系数,25℃时n为0.5),计算25℃时KF(苯酚)=_____________________。
;n为与ACF吸附能力相关的系数,25℃时n为0.5),计算25℃时KF(苯酚)=_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在20mL,0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是
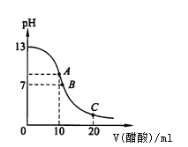
A. 在C点:c(CH3COO-)﹥c(Na+)﹥c(H+) ﹥c(OH-)
B. 在C点:c(CH3COO-)+c(CH3COOH)﹦2 c(Na+)
C. 在B点:c(OH-)﹦c(H+),c(Na+)﹦c(CH3COO-)
D. 在A点:c(Na+)﹥c(OH-)﹥c(CH3COO-)﹥c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬是一种具有战略意义的金属,它具有多种价态,单质铬熔点为1857 ℃。
(1)工业上以铬铁矿[主要成分是Fe(CrO2)2]为原料冶炼铬的流程如图所示:
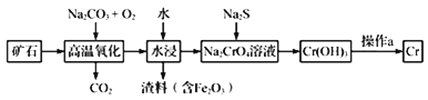
①Fe(CrO2)2中各元素化合价均为整数,则铬为_______价。
②高温氧化时反应的化学方程式为______________。
(2)Cr(OH)3是两性氢氧化物,请写出其分别与NaOH、稀硫酸反应时生成的两种盐的化学式______________。
(3)铬元素能形成含氧酸及含氧酸盐,若测得初始浓度为1 mol/L的铬酸(H2CrO4)溶液中各种含铬元素的微粒浓度为:c(CrO42-)=0.0005 mol/L、c(HCrO4-)=0.1035 mol/L、c(Cr2O72-)=a mol/L、则a =____,KHCrO4溶液中c(OH)_____c(H+)(填“>”、“<”或“=”),原因是__________________。
(4)水中的铬元素对水质及环境均有严重的损害作用,必须进行无害化处理。处理含有Cr2O72-的污水方法通常为:用铁作电极电解污水,Cr2O72-被阳极区生成的离子还原成为Cr3+,生成的Cr3+与阴极区生成的OH结合生成Cr(OH)3沉淀除去。则阴极上的电极反应式为_____,若要处理含10 mol Cr2O72-的污水,则至少需要消耗的铁为_______g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com