
| A、金属与盐溶液间的反应一定是置换反应 | ||||
| B、能与酸反应的氧化物一定是碱性氧化物 | ||||
C、
| ||||
| D、常见金属铁和铝在工业上是由热还原法制得的 |
1 1 |
1 2 |
1 1 |
1 2 |


科目:高中化学 来源: 题型:
| A、c(H+)?c(OH-)比值不变 |
| B、溶液pH增大 |
| C、c(OH-)降低了 |
| D、水电离出的c(H+)增加了 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、接触法制硫酸中采用沸腾炉的目的是为了使硫磺或黄铁矿燃烧充分,提高原料的利用率 |
| B、合成氨生产过程中采用高温高压条件都是为了提高N2、H2的转化率 |
| C、硫酸工业中,在接触室安装热交换器是为了利用硫磺或黄铁矿燃烧时放出的热量 |
| D、在联合制碱法中,参与循环的物质有CO2和NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO过量 |
| B、CO与铁矿石接触不充分 |
| C、炼铁高炉的高度不够 |
| D、CO与Fe2O3的反应有一定限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、862kJ/mol |
| B、183kJ/mol |
| C、-862kJ/mol |
| D、-183kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同系物可能互为同分异构体 |
| B、甲烷化学性质比较稳定,不能被任何氧化剂氧化 |
| C、甲烷跟氯气反应无论生成CH3Cl、CH2Cl2、CHCl3还是CCl4,都属于取代反应 |
| D、C4H10分子中四个碳原子在一条直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
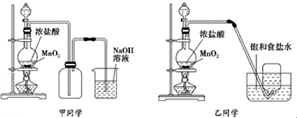
| 实验序号 | 实验操作 | 现象 | 结论 |
| ① | 加品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| ② | 加入NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
| 实验序号 | 甲 | 乙 |
| ① | ||
| ② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com