
 (1)C、N、O三种元素第一电离能从大到小的顺序是N>O>C.
(1)C、N、O三种元素第一电离能从大到小的顺序是N>O>C.分析 (1)同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第VA族元素的第一电离能大于相邻元素;
(2)根据价层电子对互斥理论确定分子空间构型;根据等电子体的定义确定等电子体;
(3)①镍属于28号元素,根据构造原理可以写出该原子的核外电子排布式;
②离子晶体的熔点与离子键的强弱有关,离子所带电荷数越多,离子半径越小,离子键越强,熔点越高;
③因为Ni0、Fe0的晶体结构类型均与氯化钠的相同,而氯化钠中阴阳离子的配位数均为6,所以Ni0晶胞中Ni和O的配位数也均为6;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,则最外层电子数为1,以此判断电子排布式;利用均摊法计算晶胞中含有的原子个数来确定原子个数之比,金属晶体中存在金属键;根据氟化钙的结构确定该晶体储氢后的化学式.
解答 解:(1)C、N、O属于同一周期元素且原子序数依次减小,同一周期元素的第一电离能随着原子序数的增大而增大,但第ⅤA族的大于第ⅥA族的,所以其第一电离能大小顺序是N>O>C,
故答案为:N>O>C;
(2)NH3分子中氮原子含有3个共价键和一个孤电子对,所以空间构型是三角锥型,与N2H4分子属于等电子体的是CH3OH(或CH3SH),
故答案为:三角锥型;CH3OH(或CH3SH);
(3)①镍属于28号元素,根据构造原理可以写出该原子的核外电子排布式,Ni的核外电子排布式是1s22s22p63s23p63d 84s2,
故答案为:1s22s22p63s23p63d 84s2;
②Ni0、Fe0的晶体结构类型均与氯化钠的相同,说明二者都是离子晶体,离子晶体的熔点与离子键的强弱有关,离子所带电荷数越多,离子半径越小,离子键越强,熔点越高.由于Ni2+的离子半径小于Fe2+的离子半径,属于熔点是NiO>FeO;
故答案为:>;
③因为Ni0、Fe0的晶体结构类型均与氯化钠的相同,而氯化钠中阴阳离子的配位数均为6,所以Ni0晶胞中Ni和O的配位数也均为6.
故答案为:6;6.
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,则最外层电子数为1,则价电子排布式为5d106s1,在晶胞中Cu原子处于面心,N(Cu)=6×$\frac{1}{2}$=3,Au原子处于顶点位置,N(Au)=8×$\frac{1}{8}$=1,则该合金中Cu原子与Au原子数量之比为3:1,为金属晶体,原子间的作用力为金属键,CaF2的结构如图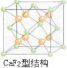 ,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中,则H原子应位于晶胞内部,则应含有8个H,则化学式为Cu3AuH8,
,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中,则H原子应位于晶胞内部,则应含有8个H,则化学式为Cu3AuH8,
故答案为:5d106s1;3:1;金属键;Cu3AuH8.
点评 本题考查了分子空间构型的判断、原子的杂化方式的判断等知识点,难度不大,注意分子空间构型的判断及原子杂化方式的判断是高考的热点.


科目:高中化学 来源: 题型:选择题
| A. | 氨气通入醋酸溶液 CH3COOH+NH3═CH3COONH4 | |
| B. | 澄清的石灰水与盐酸反应:H++OH-═H2O | |
| C. | 碳酸钡加入稀硫酸:BaCO3+2H+═Ba2++H2O+CO2↑ | |
| D. | 氯气通入水中:Cl2+H2O═2H++Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯中所有原子都处于同一平面内 | |
| B. | 甲烷和乙烯都可以与氯气反应 | |
| C. | 酸性高锰酸钾溶液可以氧化苯和甲烷 | |
| D. | 乙烯可以与氢气发生加成反应,苯不能与氢气加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
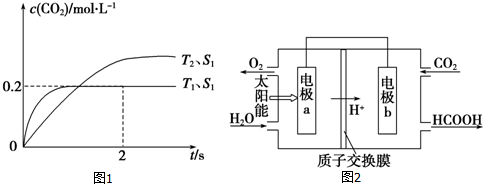
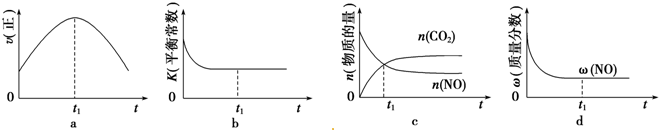
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)元素M是短周期元素,其常量存在于海水中,单质被誉为“国防金属”.
(1)元素M是短周期元素,其常量存在于海水中,单质被誉为“国防金属”.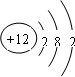 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com