
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
X | Y | Z | |
① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
② | KOH溶液 | SiO2 | 浓盐酸 |
③ | O2 | N2 | H2 |
④ | FeCl3溶液 | Cu | 浓硝酸 |
A.①③ B.①④ C.②④ D.②③
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源:2017届辽宁省铁岭市协作体高三第三次联考化学试卷(解析版) 题型:选择题
在固态金属氧化物电解池中,高温共电解H2O—CO 2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是( )
2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是( )

A.X是电源的负极
B.阴极的反应式是:H2O +2eˉ=H2+O2ˉ、CO2+2eˉ=CO+O2ˉ
+2eˉ=H2+O2ˉ、CO2+2eˉ=CO+O2ˉ
C.总反应可表示为:H2O+CO2 H2+CO+O2
H2+CO+O2
D.阴、阳两极生成的气体的物质的量之比是1︰1
查看答案和解析>>
科目:高中化学 来源:2017届江西省、兴国三中等四校高三上第一次联考化学卷(解析版) 题型:选择题
铋(Bi) 位于元素周期表中第ⅤA族,其价态为+3价时较稳定,铋酸钠(NaBiO3)溶液呈无色。现取一定量的硫酸锰(MnSO4)溶液,向其中依次滴加下列溶液,对应实验现象如表所示:
位于元素周期表中第ⅤA族,其价态为+3价时较稳定,铋酸钠(NaBiO3)溶液呈无色。现取一定量的硫酸锰(MnSO4)溶液,向其中依次滴加下列溶液,对应实验现象如表所示:
加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI?淀粉溶液 |
实验现象 | 溶液呈紫红色 | 溶液紫红色消失,产生气泡 | 溶液变成蓝色 |
则NaBiO3、KMnO4、I2、H2O2的氧化性由强到弱的顺序为( )
A.I2、H2O2、KMnO4、NaBiO3 B.H2O2、I2、NaBiO3、KMnO4
C.NaBiO3、KMnO4、H2O2、I2 D.KMnO4、NaBiO3、I2、H2O2
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上期中化学试卷(解析版) 题型:选择题
目前处理酸性Cr2O72-废水多采用铁氧磁体法,该法是向废水中加入FeSO4 ·7H2O将Cr2O72-还原成Cr3+,调节pH,Fe、Cr转化成相当于: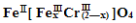
 (铁氧磁体,罗马数字表示元素价态)的沉淀。处理1mol Cr2O72-,需加入a mol FeSO4 • 7H2O,下列结论正确的是( )
(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1mol Cr2O72-,需加入a mol FeSO4 • 7H2O,下列结论正确的是( )
A.x =0.5,a =8  B.x =0.5 ,a = 10
B.x =0.5 ,a = 10
C.x = 1.5,a =8 D.x = 1.5 ,a = 10
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上期中化学试卷(解析版) 题型:选择题
下列实验操作能达到实验目的的是
实验目的 | 实验操作 | |
A. | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和FeCl3溶液中 |
B. | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液加热蒸干 |
C. | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
D. | 比较水与乙醇中氢的活泼性 | 分别将少量钠投入到盛有水和乙醇的烧杯中 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省等三校高二上期中化学卷(解析版) 题型:填空题
超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO(g)+2CO(g)  2CO2(g)+N2(g)。为了测定在某种催化剂作用下的反应速率,T℃时用气体传感器测得恒容密闭容器中不同时间下的NO和CO浓度,其数据如下表(不考虑温度变化对催化剂催化效率的影响)
2CO2(g)+N2(g)。为了测定在某种催化剂作用下的反应速率,T℃时用气体传感器测得恒容密闭容器中不同时间下的NO和CO浓度,其数据如下表(不考虑温度变化对催化剂催化效率的影响)
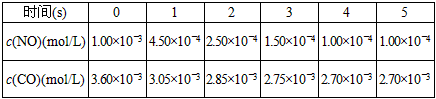
(1)达到平衡后,升高温度,N2的反应速率__________(填“增大”“减小”或“不变”)。
(2)T℃时,CO的平衡转化率为_________;增大压强,NO的平衡转化率__________(填“增大”“减小”或“不变”)。
(3)已知NO的键能为632kJ/mol,CO的键能为1075kJ/mol,C=O的键能为803kJ/mol,N≡N的键能为946kJ/mol,则△H=___________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省等三校高二上期中化学卷(解析版) 题型:选择题
室温下,浓度均为0.2 mol/L的HA和BOH溶液等体积混合后,所得溶液中部分粒子组分及浓度如图所示。下列说法中不正确的是
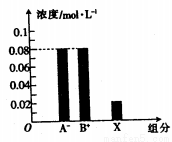
A.HA、BOH均为弱电解质 B. X表示HA或BOH分子
C. 电离常数 K(HA)=K(BOH) D.该盐溶液pH=4.53
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海师大附中高一上期中化学试卷(解析版) 题型:填空题
(1)水(H2O)在很多化学反应中具有极其重要的作用。请研究下列水参与的氧化还原反应。 ①NaH+H2O=NaOH+H2↑
②2Na2O2+2H2O=4Na OH+O2↑
OH+O2↑
③2Na+2H2O =2NaOH+H2↑
④3NO2+H2O=2HNO3+NO
⑤2H2O 2H2↑+O2↑
2H2↑+O2↑
⑥2F2+2H2O=4HF+O2
水只作氧化剂的是____________;水只作还原剂的是____________;水既作氧化剂,又作还原剂的是____________;水既不作氧化剂,又不是还原剂的是____________。
(2)KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为:2KClO3+4HCl (浓)=2KCl+2ClO2↑+Cl2↑+2H2O。
①请分析该反应中电子转移的情况(用双线桥法表示)。
②浓盐酸在反应中显示出来的性质是________(填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③若产生0.1 mol Cl2,则转移的电子的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上期中化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式,正确的是
A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B.硝酸亚铁溶液中滴加少量稀硫酸:Fe2++NO3-+4H+=Fe3++NO↑+2H2O
C.把反应Cu+2FeCl3=2FeCl2+CuCl2设计成原电池,其正极反应为Fe3++e-=Fe2+
D.向硫酸氢钠溶液中加入氢氧化钡溶液至中性,则离子方程式为H++SO42-+OH-=BaSO4↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com