
合成氨是重要的化学工业,为了研究合成氨的反应原理,在一密闭容器内充入1 mol N2和2 mol H2,在一定条件下,使之发生如下反应:N2+3H2  2NH3 。
2NH3 。
Ⅰ:若维持温度不变,且密闭容器的容积固定为1 L。
(1) 当此反应经过2 min达到平衡状态时,测得反应混合物中NH3的物质的量为0.2 moL,则H2在2 min内的平均反应速率为__________________。
(2)如果开始时,向该容器内加入0.5 moL N2 ,要使反应混合物中三种气体的物质的量分数仍与上述平衡时的完全相同,则还必须加入H2 _______mol和NH3 _______mol。
(3)如果开始时加入N2、H2、NH3的物质的量分别为a mol 、b mol 、c mol ,要使反应达到平衡状态时,反应混合物中三种气体的物质的量分数仍与(1)平衡时完全相同,则a、b、c应满足的一般条件是(a、b分别用含c的方程式表示) 。
Ⅱ:若温度维持不变,体系压强维持与Ⅰ相同,密闭容器的容积由1 L随反应进行而改变。
(4)开始时加入1 mol N2和2 mol H2,经过一段时间,容器中三种气体的物质的量分数不再发生变化时,则NH3的物质的量为__________(选填一个编号)
(甲)大于0.2 mol (乙)等于0.2 mol
(丙)小于0.2 mol (丁)可能大于、等于或小于0.2mol
作出此判断的理由是__________________________________________。
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源:2012-2013学年河北枣强中学高二上学期期末考试化学试卷(带解析) 题型:填空题
已知下列反应(反应所需的其他条件和各物质的化学计量数均已略去):
①A+B  M+D+E;②E+M=A+F+B
M+D+E;②E+M=A+F+B
请回答:
(1)若A是一种钠盐,该反应是化学工业上制单质E和化合物M的重要方法。该化学工业称为 (填字母编号:a.硫酸工 业 b.氯碱工业 c.合成氨工业d.侯氏制碱工业),写出上述反应②的离子方程式为__________ 。
(2)若A是一种含氧酸盐,该反应中电极上会析出红色固体。则其电解反应方程式是: 。上述两种不同反应中的产物E((1)题)和产物F((2)题)有一种共同的用途是__ ____, 二者反应的离子方程式为______________ __。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年河北省遵化市高二上学期期中质量检测化学试卷(解析版) 题型:填空题
氮是地球上含量丰富的一种元素,氮及其化合物在工 农业生产、生活中有着重要作用,
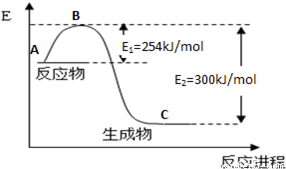
(1)上图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式: 。
(2)若已知下列数据:
|
化学键 |
H-H |
N≡N |
|
键能/kJ·mol-1 |
435 |
943 |
试根据表中及图中数据计算N-H的键能 kJ·mol-1。
(3)合成氨反应通常用铁触媒作催化剂。使用铁触媒后E1和E2的变化是:E1 ,E2______,
△H (填“增大”、“减小”、“不变”)。
(4)用NH3催化还原NOX还可以消除氮氧化物的污染。例如
4NH3(g)+3O2(g)= 2N2(g)+6H2O(g) ;△H1=akJ·mol-1
N2(g)+O2(g)=2NO(g); △H2=bkJ/mol
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3= kJ/mol(用含a、b的式子表示)。
查看答案和解析>>
科目:高中化学 来源:2014届河北枣强中学高二上学期期末考试化学试卷(解析版) 题型:填空题
已知下列反应(反应所需的其他条件和各物质的化学计量数均已略去):
①A+B  M+D+E;②E+M=A+F+B
M+D+E;②E+M=A+F+B

请回答:
(1)若A是一种钠盐,该反应是化学工业上制单质E和化合物M的重要方法。该化学工业称为 (填字母编号:a.硫酸工 业 b.氯碱工业 c.合成氨工业d.侯氏制碱工业),写出上述反应②的离子方程式为__________ 。
(2)若A是一种含氧酸盐,该反应中电极上会析出红色固体。则其电解反应方程式是: 。上述两种不同反应中的产物E((1)题)和产物F((2)题)有一种共同的用途是__ ____, 二者反应的离子方程式为______________ __。
查看答案和解析>>
科目:高中化学 来源:四川省模拟题 题型:填空题
 2NH3(g);△H= -92.4 kJ/mol,
2NH3(g);△H= -92.4 kJ/mol,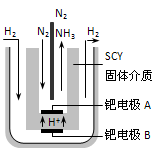
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com