
| A. | 含有NA个氖原子的氖气在标准状况下的体积约为11.2 L | |
| B. | 30 g乙烷中含共用电子对总数为8NA | |
| C. | 常温常压下,11.2 L氮气所含的原子数目为NA | |
| D. | 常温下,0.05 mol CO2和SO2混合气体中所含氧原子数为0.1NA |
分析 A.氖气是单原子分子;
B.求出乙烷的物质的量,然后根据乙烷中含7对共用电子对来分析;
C.气体摩尔体积标准状况下为22.4L/mol;
D.根据二氧化碳和二氧化硫的物质的量及分子组成计算出含有的氧原子数目.
解答 解:A.氖气是单原子分子,含有NA个氖原子的氖气物质的量为1mol,在标准状况下的体积约为22.4L,故A错误;
B.30g乙烷的物质的量为1mol,而乙烷中含7对共用电子对,故1mol乙烷中含7NA对共用电子对,故B错误;
C.常温常压下,11.2 L氮气物质的量不是0.5mol,故C错误;
D.0.05mol二氧化碳和二氧化硫的混合气体中含有0.1mol氧原子,所含氧原子数为0.1NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件分析,物质的量计算微粒数,注意醋酸是弱电解质,氖气是单原子分子,掌握基础是关键,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题

| A. | 若此反应过程中有电子转移,可设计成原电池 | |
| B. | 该反应为放热反应 | |
| C. | 该反应在常温下也有可能进行 | |
| D. | 反应物的总能量高于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以海水为原料制得精盐,再电解精盐的水溶液制取钠 | |
| B. | 用海水、石灰乳等为原料,经一系列过程制得氧化镁,用H2还原氧化镁制得镁 | |
| C. | 以铁矿石、焦炭、空气、石灰石等为原料,通过反应产生的CO在高温下还原铁矿石制得铁 | |
| D. | 从铝土矿中获得氧化铝再制得氯化铝固体,电解熔融的氯化铝得到铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ①③⑤ | C. | ③④⑤ | D. | ④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯乙烯和聚乙烯均能发生加成反应 | |
| B. |  和 和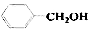 互为同系物 互为同系物 | |
| C. | 用新制氢氧化铜悬浊液能鉴别葡萄糖和乙酸 | |
| D. | 等质量的乙烯和乙醇完全燃烧,消耗氧气的物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素X、Z组成的化合物中,离子个数比为1:1 | |
| B. | W的简单气态氢化物的热稳定性比Y的强 | |
| C. | 由X、W两种元素组成的化合物中,其中一种具有漂白性 | |
| D. | 原子半径:r(X)<r(Y)<r(Z)<r(W) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:A>D>B>C | B. | 原子半径:D>B>C>A | ||
| C. | 原子序数:C>D>B>A | D. | 简单离子半径:A>B>C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑥ | B. | ②④⑤ | C. | ①②③④ | D. | ⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40% | B. | 20% | C. | 15% | D. | 60% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com