
【题目】全钒电池以惰性材料作电极,在电解质溶液中发生的电池总反应为:
VO2+(蓝色)+H2O+V3+(紫色)![]() VO2+(黄色)+V2+(绿色)+2H+
VO2+(黄色)+V2+(绿色)+2H+
下列说法错误的
A. 充电时,反应每生成2mol H+时电子转移的物质的量为2mol
B. 放电过程中,正极附近溶液的酸性减弱
C. 放电时,正极反应为VO2++2H++e-=VO2++H2O
D. 充电时,阳极附近溶液由蓝色逐渐变为黄色
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
【题目】如图甲是利用一种微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是( )
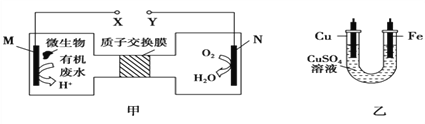
A. 铜电极应与X相连接
B. H+透过质子交换膜由右向左移动
C. M电极反应式为CO(NH2)2+H2O-6e-===CO2↑+N2↑+6H+
D. 当N电极消耗0.25 mol气体时,则理论上铁电极增重16 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l) H=-632kJ·mol-1。下图为质子膜H2S燃料电池的示意图。下列说法错误的是( )
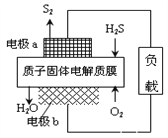
A. 电池工作时,电子从电极a经负载流向电极b
B. 实际工作中当反应生成64gS2时,电池内部释放632kJ电能
C. 电极a上发生的电极反应为:2H2S - 4e-=S2 + 4H+
D. 当电路中通过4mol电子时,有4molH+经质子膜进入正极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。 右图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。下列说法不正确的是( )

A. 腐蚀过程中,负极是c
B. 正极反应是 O2+ 4e-+2H2O = 4OH-
C. 若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为0.224L(标准状况)
D. 环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羊通过吃草获得化合物和元素,那么羊和草体内的各种化学元素( )
A. 种类差异很大,含量大体相同 B. 种类和含量差异都很大
C. 种类大体相同,含量差异很大 D. 种类和含量都是大体相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中Cl-的物质的量浓度最大的是
A.200mL 2mol·L—1MgCl2溶液B.500mL 2.5mol·L—1NaCl溶液
C.30mL 2.5mol·L—1CaCl2溶液D.250mL 1mol·L—1AlCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,A与B可形成BA型化合物,且A元素是卤族元素中非金属性最强的元素;金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8;C元素有3种同位素C1、C2、C3,自然界中含量最多的是C1,C3原子的质量数是C1的3倍,C2原子的质量数是C1的2倍;D的气态氢化物的水溶液呈碱性;而其最高价氧化物对应的水化物为强酸;E元素原子的最外层电子数比次外层电子数多4。
(1)写出下列元素的元素符号:A.________,B.______,C.________,D.________,E.________。
(2)写出C1、C2、C3三种原子的符号:C1________,C2________,C3________。
(3)E2-的结构示意图为________。
(4)A与B形成的化合物的化学式是_______,最常见的E原子与C2形成的分子中含________个中子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月18日中共中央国务院公开致电祝贺南海北部神狐海域进行的“可燃冰”试采成功。“可燃冰”是天然气水合物,外形像冰,在常温常压下迅速分解释放出甲烷,被称为未来新能源。
(1)“可燃冰”作为能源的优点是__________(回答一条即可)。
(2)甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整两个过程。向反应系统同时通入甲烷,氧气和水蒸气,发生的主要化学反应如下:
反应过程 | 化学方程式 | 焓变△H(kJ.mol-l) | 活化能E.(kJ.mol-1) |
甲烷氧化 | CH4(g)+O2(g) | -802.6 | 125.6 |
CH4(g)+O2(g) | -322.0 | 172.5 | |
蒸气重整 | CH4(g)+H2O(g) | +206.2 | 240.1 |
CH4(g)+2H2O(g) | +158.6 | 243.9 |
回答下列问题:
①在初始阶段,甲烷蒸汽重整的反应速率______(填“大于”“小于”或“等于”)甲烷氧化的反应速率。
②反应CH4(g)+H2O(g)![]() CO(g)+3H2(g)的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。
CO(g)+3H2(g)的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。

该反应在图中A点的平衡常数Kp=________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),图中压强(p1、p2、p3、p4)由大到小的顺序为___________。
③从能量角度分析,甲烷自热重整方法的先进之处在于___________。
④如果进料中氧气量过大,最终会导致H2物质量分数降底,原因是__________。
(3)甲烷超干重整CO2技术可得到富含CO的气体,其能源和开境上的双重意义重大,甲烷超干重整CO2的催化转化原理如图所示。

①过程II中第二步反应的化学方程式为_____________。
②只有过程I投料比![]() _______,过程II中催化剂组成才会保持不变。
_______,过程II中催化剂组成才会保持不变。
③该技术总反应的热化学方式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质按纯净物、混合物、电解质、非电解质的顺序排列的是( )
A.纯碱、稀盐酸、氢氧化钠、干冰B.醋酸、盐酸、铜、氨气
C.石灰石、石油、水、硫酸钡D.烧碱、海水、氯化钠、氯气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com