
分析 单质A与水蒸气反应生成B,B溶于盐酸生成C(棕黄色)和D(浅绿色)的混合物,即B溶于盐酸后反应后得到含Fe3+和Fe2+的溶液,据此可知A、B、C、D;要除去Fe2+中的Fe3+,应利用发生2Fe3++Fe=3Fe2+来分析;若除去FeCl3中的FeCl2,应加入氯气做氧化剂;Fe3+的检验用KSCN溶液,生成血红色Fe(SCN)3;检验Fe3+中的Fe2+,用KMnO4溶液,在酸性条件下能被Fe2+还原而褪色来检验.
解答 解:单质A与水蒸气反应生成B,B溶于盐酸生成C(棕黄色)和D(浅绿色)的混合物,即B溶于盐酸后反应后得到含Fe3+和Fe2+的溶液,据此可知B为Fe3O4,C为FeCl3,D为FeCl2;要除去Fe2+中的Fe3+,应利用加入铁饭能发生2Fe3++Fe=3Fe2+,既能除去Fe3+还不引入杂质;若除去FeCl3中的FeCl2,应加入氯气做氧化剂,能将Fe2+氧化为Fe3+:2Fe2++Cl2=2Fe3+;Fe3+的检验用KSCN溶液,生成血红色Fe(SCN)3:Fe3++3SCN-=Fe(SCN)3;检验Fe3+中的Fe2+,用KMnO4溶液,在酸性条件下能被Fe2+还原而褪色:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.故答案为:铁粉;2Fe3++Fe=3Fe2+;氯气;2Fe2++Cl2=2Fe3+;KSCN溶液;Fe3++3SCN-=Fe(SCN)3;高锰酸钾溶液;5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
点评 本题考查了铁的氧化物与酸的反应产物的检验和除杂,难度不大,应注意的是铁离子的检验用KSCN溶液.


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:选择题
| A. | SO2漂白纸浆 | B. | 纯碱清洗油污 | ||
| C. | Na2S除污水中的Cu2+ | D. | 漂白粉漂白织物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
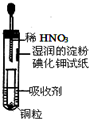
| A. | 吸收剂可以是NaOH溶液 | B. | 试管上部的气体始终为无色 | ||
| C. | 小试管中溶液最终呈蓝色 | D. | 试纸先变红后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 色态 | 溶于碱 | 超过1kPa受热 或遇光 | |
| 常温气体 | -59-11℃红黄色液体 | 生成亚氯酸盐和氯酸盐 | 爆炸 |
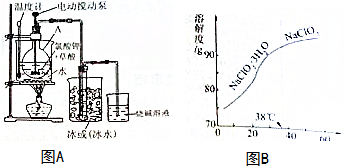
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验设计及操作 | 离子方程式 |
| Ⅰ.向盛有2mlCuSO4溶液的试管里加入2mlNaOH溶液,观察现象 | Cu2++2OH-═Cu(OH)2↓ |
| Ⅱ.向盛有2mL pH=1的HCl溶液的试管里慢慢滴入18mL(已足量)CH3COONH4溶液(查资料知CH3COONH4,溶液呈中性 )震荡摇匀,测得pH≈3.7 | |
| Ⅲ向盛有2mLNaHCO3溶液的试管里加入2mL H2SO4溶液,观察现象 | HCO${\;}_{3}^{-}$+H+═H2O+CO2↑ |
| Ⅳ向盛有2mL 稀Na2SO4溶液的试管里加入2mL稀KCl溶液,观察无明显现象 |  |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
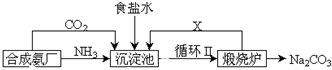
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

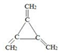 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验必需仪器有滴定管、锥形瓶、滴定管夹架台 | |
| B. | 若选择甲基橙作指示剂,则测得食醋中CH3COOH浓度偏高 | |
| C. | 滴定之前的操作是选滴管、检漏、水洗、润洗、装液、调液面、读数 | |
| D. | 开始俯视读数,终点时仰视读数,测得食醋中CH3COOH浓度偏高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com