
【题目】某小组同学利用原电池装置探究物质的性质。
资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。
(1)同学们利用下表中装置进行实验并记录。
装置 | 编号 | 电极A | 溶液B | 操作及现象 |
| I | Fe | pH=2的 H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
Ⅱ | Cu | pH=2的 H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
①同学们认为实验I中铁主要发生了析氢腐蚀,其负极反应式是__________。
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其理论判断依据是__________;
乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是__________。
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性的因素。
编号 | 溶液B | 操作及现象 |
Ⅲ | 经煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
V | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
①丙同学比较实验II、Ⅲ、Ⅳ的电压表读数为:c>a>b,请解释原因是__________。
②丁同学对Ⅳ、V进行比较,其目的是探究__________对O2氧化性的影响。
③实验Ⅳ中加入Na2SO4溶液的目的是__________。
④为达到丁同学的目的,经讨论,同学们认为应改用下图装置对Ⅳ、V重复进行实验,其设计意图是__________;重复实验时,记录电压表读数依次为c'、d',且c'>d',由此得出的结论是__________。
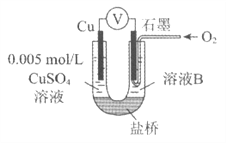
【答案】 Fe—2e-=Fe2+ 在金属活动性顺序中,Cu在H后,Cu不能置换出H2 O2+4H++4e-=2H2O O2浓度越大,其氧化性越强,使电压值增大 溶液的酸碱性 排除溶液中的Na+(或SO42-)对实验的可能干扰 排除Cu在酸碱性不同的溶液中,其还原性不同对该实验结果的影响 溶液酸性越强,O2的氧化性越强(介质或环境的pH影响物质的氧化性)
【解析】分析:(1).①.I中的铁主要发生析氢腐蚀,铁在负极失电子发生氧化反应;②.铜与氢离子不能发生自发的氧化还原反应;乙同学认为实验Ⅱ中应发生吸氧腐蚀,则在正极上氧气得电子发生还原反应生成水;(2). ①.实验Ⅱ、Ⅲ、IV的电解质相同,不同的是氧气的浓度,出现了电压表读数不同,根据数值的相对大小可知,氧气浓度越大,电压表的读数越高;②.实验Ⅳ、V是利用电解质溶液的酸碱性不同,来判断电压表的指针偏转情况;③.实验IV中加入Na2SO4溶液的目的是排除溶液中的Na+(或SO42-)对实验的可能干扰;④.为达到丁同学的目的,经讨论,同学们认为应改用如图装置对IV、V重复进行实验,其设计意图是排除Cu在酸碱性不同的溶液中,其还原性不同对该实验结果的影响;重复实验时,记录电压表读数依次为c'、d',且c'>d',说明溶液酸性越强,O2的氧化性越强。
详解:(1). ①. I中的铁主要发生析氢腐蚀,则铁在负极失电子发生氧化反应,电极反应式为:Fe-2e-=Fe2+,故答案为:Fe-2e-=Fe2+;
②. 在金属活动性顺序中,Cu在H的后面,铜与氢离子不能发生自发的氧化还原反应;乙同学认为实验Ⅱ中应发生吸氧腐蚀,则在正极上氧气得电子发生还原反应生成水,其正极的电极反应式是O2+4H++4e-=2H2O,故答案为:在金属活动性顺序中,Cu在H后,Cu不能置换出H2;O2+4H++4e-=2H2O;
(2). ①. 实验Ⅱ、Ⅲ、IV的电解质相同,不同的是氧气的浓度,出现了电压表读数不同,根据数值的相对大小可知,氧气浓度越大,电压表的读数越高,所以O2浓度越大,其氧化性越强,使电压值增大,故答案为:O2浓度越大,其氧化性越强,使电压值增大;
②. 在实验Ⅳ、V中是利用溶液的酸碱性不同来判断电压表的指针偏转情况,所以Ⅳ、V进行比较,其目的是探究溶液的酸碱性对O2氧化性的影响,故答案为:溶液的酸碱性;
③. 实验IV中加入Na2SO4溶液的目的是排除溶液中的Na+(或SO42-)对实验的可能干扰,故答案为:排除溶液中的Na+(或SO42-)对实验的可能干扰;
④. 为达到丁同学的目的,经讨论,同学们认为应改用如图装置对Ⅳ、V重复进行实验,其设计意图是排除Cu在酸碱性不同的溶液中,其还原性不同对该实验结果的影响;重复实验时,记录电压表读数依次为c'、d',且c'>d',由此得出的结论是溶液酸性越强,O2的氧化性越强,故答案为:排除Cu在酸碱性不同的溶液中,其还原性不同对该实验结果的影响;溶液酸性越强,O2的氧化性越强(介质或环境的pH影响物质的氧化性)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】以冶铝的废弃物铝灰为原料制取超细α氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下图:
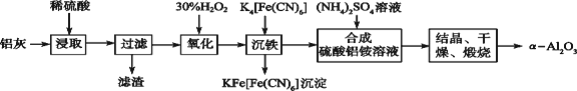
(1)写出铝灰与氢氧化钠溶液反应涉及的化学方程式:_______________________。
(2)加30%H2O2溶液发生的离子反应方程式为______________________________。
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]![]() 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
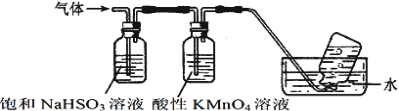
集气瓶中收集到的气体是_______(填化学式)。
②酸性KMnO4溶液紫色变浅_______(填“能”或“不能”)说明煅烧硫酸铝铵晶体产物中含有SO2气体?理由:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计实验验证以下规律:元素的非金属性越强,对应的最高价氧化物的水化物酸性就越强。该小组设计了如图装置进行实验。拟比较C、Si、S三种元素的非金属性。
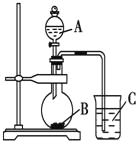
(1)推测三种元素对应的最高价氧化物的水化物酸性由强到弱的顺序是_________________(填化学式)。
(2)若B、C均为正盐,且焰色反应均为黄色。A、B、C的化学式依次为_________、__________、_________(A、C填溶质的化学式)。
(3)烧瓶中的实验现象为________________________________。
(4)固体B也可以用B的溶液代替。实验室配制0.1mol/L的B的溶液450mL,需要用托盘天平称取B_____g。
(5)有同学认为,将A中物质换为浓硝酸,其余试剂不变。则可以验证N、C、Si三元素的非金属性强弱。你认为,该同学的观点___________(选填“正确”“错误”)。理由是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是( )
A. 硫离子的结构示意图:![]()
B. 明矾的化学式:KAlSO412H2O
C. 亚硫酸的电离方程式:H2SO3=2H++SO32﹣
D. 质子数为17、中子数为20的氯原子:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图。下列叙述正确的是( )
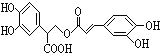
A. 迷迭香酸属于芳香烃
B. 迷迭香酸含有五种官能团
C. 1mol迷迭香酸最多能和7mol溴水发生反应
D. 1mol迷迭香酸最多能和含6mol NaOH的水溶液完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素。下列判断错误的是 ( )
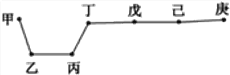
A. 甲可能是金属元素
B. 气态氢化物的稳定性:庚>己>戊
C. 丙与戊的最高价氧化物的水化物可以相互反应
D. 庚的最高价氧化物的水化物酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中不正确的是( )
A.工业上可利用海水制取镁
B.从海产品(如海带等)中提取碘是工业上获取碘的重要途径
C.工业上可通过铝土矿获得铝
D.工业上用CO氧化赤铁矿(含Fe2O3)获得铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V2﹣、W3﹣、X2+、Y2﹣、Z﹣是由短周期元素形成的简单离子,其中V2﹣、W3﹣、X2+均是10电子的微粒,Y2﹣、Z﹣与Ar原子具有相同的电子数。(请用化学用语回答下列问题)
(1)V2﹣的离子结构示意图为_________________。
(2)V、W、X的原子半径由小到大的顺序是________________。
(3)元素Y、Z气态氢化物的热稳定性比较(填化学式):______________。
(4)将Z的单质通入石蕊溶液中发生的颜色变化如下图,请在方框内填写出导致该阶段颜色变化的主要粒子符号。________、________、________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某一化学反应中,反应物B的浓度在5 s内从2.0 mol/L变成0.5 mol/L,在这5 s内B的化学反应速率为
A. 0.3B. 0.3 mol/(L·s)
C. 0.4 mol(L·s)-1D. 0.04 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com