
某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L H2SO4溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
若实验中大约要使用245 mL NaOH溶液,则至少需要称量NaOH固体________g。
Ⅱ.测定中和热的实验装置如图所示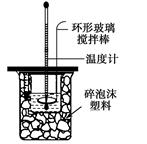
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值57.3 kJ/mol):________ 。
(2)取50 mL NaOH溶液和30 mL硫酸进行实验,实验数据如下表。
①请填写下表中的空白: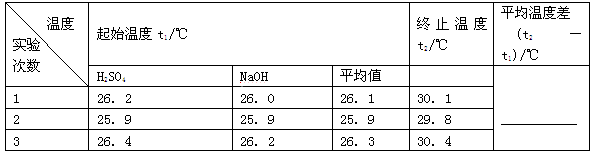
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L H2SO4溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热ΔH=________(取小数点后一位)。
③上述实验结果的数值与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)________。
a.实验装置保温、隔热效果差
b.在量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
Ⅰ. 5.0
Ⅱ.(1)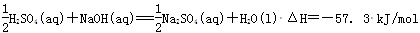 。
。
(2)①4.0 ②-53.5 kJ/mol ③acd
解析试题分析:Ⅰ、要使用245 mL NaOH溶液,需要配制250mL溶液,所以需要氢氧化钠
m=cvM=0.50×0.25×40=5.0g;
Ⅱ、(1)中和热是指稀强酸和稀强碱反应生成1mol水所放出的能量,稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式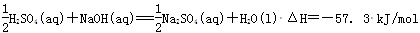 ;(2)①根据表中数据,平均温差4.0℃;②根据题意,生成0.025mol水放出热量为4.18×80×4=1337.6J,生成1mol水放出热量为1.3376kJ÷0.025=53.504 kJ,中和热ΔH=-53.5kJ/mol。③隔热效果差,热量散失实验结果偏低;量取NaOH溶液的体积时仰视读数,量取的氢氧化钠偏多,实验结果偏高;分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中,热量散失多,实验结果偏低;用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度,氢氧化钠和硫酸反应放热,使硫酸起始温度升高,温差缩小实验结果偏低,产生偏差的原因可能是acd
;(2)①根据表中数据,平均温差4.0℃;②根据题意,生成0.025mol水放出热量为4.18×80×4=1337.6J,生成1mol水放出热量为1.3376kJ÷0.025=53.504 kJ,中和热ΔH=-53.5kJ/mol。③隔热效果差,热量散失实验结果偏低;量取NaOH溶液的体积时仰视读数,量取的氢氧化钠偏多,实验结果偏高;分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中,热量散失多,实验结果偏低;用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度,氢氧化钠和硫酸反应放热,使硫酸起始温度升高,温差缩小实验结果偏低,产生偏差的原因可能是acd
考点:本题考查溶液配制、中和热测定。


科目:高中化学 来源: 题型:单选题
下列有关物质制备的说法中正确的是
| A.工业上通过电解MgO制取镁 |
| B.工业上通过向浓缩的海水中通入氯气获得碘 |
| C.工业上主要通过高温冶炼黄铜矿获得铜 |
| D.工业上用二氧化锰与浓盐酸制备氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
道尔顿的原子学说曾经起了很大作用。他的学说中,包含有下述三个论点:①原子是不能再分的粒子;②同种元素的原子的各种性质和质量都相同;③原子是微小的实心球体。从现代观点看,你认为这三个论点中不确切的
| A.只有③ | B.只有①③ | C.只有②③ | D.有①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在下列变化过程中,被破坏的作用力正确的是
| A.干冰升华一一共价键 |
| B.二氧化硅熔融——范德华力 |
| C.氢氧化钠熔融——离子键、共价键 |
| D.硫酸氢钠溶于水——离子键、共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(14分)中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是______,烧杯间填满碎塑料泡沫的作用是______。
(2)大烧杯上如不盖硬纸板,则求得的中和热数值_________(填“偏大”、“偏小’、“无影响”)
(3)实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”理由是________________;所求中和热的数值会________(填“相等”或“不相等”),理由是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(8分)50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
(1)烧杯间填满碎泡沫塑料的作用是_______________________________________________。
(2)大烧杯上如不盖硬纸板,求得的中和热数值________(填“偏大”“偏小”“无影响”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸进行反应,与上述实验相比,所放出的热量________(填“相等”、“不相等”),所求中和热__________(填“相等”、“不相等”),
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某温度下,反应SO2(g)+  O2(g)
O2(g) SO3 (g) 的平衡常数K1=50,在同一温度下,反应SO3(g)
SO3 (g) 的平衡常数K1=50,在同一温度下,反应SO3(g) SO2(g) +
SO2(g) +  O2(g)的平衡常数K2的值为
O2(g)的平衡常数K2的值为
| A.2500 | B.100 | C.0.02 | D.0.001 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将纯水加热至较高温度,下列叙述正确的是
| A.水的离子积变大、pH变小、呈酸性 | B.水的离子积不变、pH不变、呈中性 |
| C.水的离子积变小、pH变大、呈碱性 | D.水的离子积变大、pH变小、呈中性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com