
【题目】向200.0mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应.在上述所得溶液中,逐滴缓慢滴加2.0molL﹣1的盐酸,所得气体(不考虑溶解)的体积与滴加盐酸的体积关系如图(其中点A是线段OC上的动点):
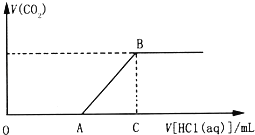
(1)若OA=AC时,通入CO2后,所得溶液的溶质成分是 ________________.
(2)若OA>AC时,OA段发生反应的离子方程式是________________________________
(3)若A点数值为80,C点数值为260,试确定通入CO2后得到的溶液溶质成 分及其物质的量浓度.(有几种填几种,不必填满,成分用化学式表示)
①成分1:________________物质的量浓度:________
②成分2:_______________ 物质的量浓度:_________
③成分3:_______________ 物质的量浓度:_________
④成分4:______________ _物质的量浓度:_________
【答案】Na2CO3 2 OH﹣+H+=H2O CO32﹣+H+=HCO3﹣ 3 (顺序可以颠倒) Na2CO3 0.8mol/L NaHCO3 1.0mol/L
【解析】
NaOH溶液中缓慢通入一定量的CO2,充分反应,所得溶液,可以是碳酸钠,还可以是碳酸氢钠,还可以是碳酸钠和氢氧化钠的混合物,或是碳酸氢钠和碳酸钠的混合物,与盐酸先后发生的反应依次是:NaOH+HCl=NaCl+H2O,Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+H2O+CO2↑,以此解答。
(1) AC段有气体二氧化碳生成,AC段的反应是NaHCO3+HCl═NaCl+H2O+CO2↑,根据碳元素守恒,若OA=AC,则OA段只发生Na2CO3+HCl═NaHCO3+NaCl反应,则通入CO2后,所得溶液的溶质成分是Na2CO3;
(2) AC段有气体二氧化碳生成,AC段的反应是NaHCO3+HCl═NaCl+H2O+CO2↑,若OA>AC,则OA段依次发生NaOH+HCl=NaCl+H2O、Na2CO3+HCl═NaHCO3+NaCl反应,溶液的组成是氢氧化钠和碳酸钠的化合物,OA段反应离子方程式依次是OH﹣+H+=H2O (4). CO32﹣+H+=HCO3﹣;
(3)若A点数值为80,C点数值为260,OA<AC,所以溶质是碳酸钠和碳酸氢钠的混合物,在OA段发生反应是Na2CO3+HCl═NaHCO3+NaCl,消耗盐酸的物质的量为:2.0mol/L×0.08L=0.16mol,所以碳酸钠的物质的量是0.16mol,碳酸钠的浓度是:![]() 0.8mol/L,在AC段消耗盐酸的物质的量是2.0mol/L×(0.26-0.08)L=0.36mol,AC段发生的反应是NaHCO3+HCl═NaCl+H2O+CO2↑,OA段反应生成的碳酸氢钠是0.16mol,所以原来的混合液中含有的碳酸氢钠是0.36mol-0.16mol=0.20mol,所以碳酸氢钠的浓度
0.8mol/L,在AC段消耗盐酸的物质的量是2.0mol/L×(0.26-0.08)L=0.36mol,AC段发生的反应是NaHCO3+HCl═NaCl+H2O+CO2↑,OA段反应生成的碳酸氢钠是0.16mol,所以原来的混合液中含有的碳酸氢钠是0.36mol-0.16mol=0.20mol,所以碳酸氢钠的浓度![]() 1.0mol/L。
1.0mol/L。


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】(12分)已知某溶液中存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,则该溶质是________,上述四种离子浓度的大小顺序为________(选填序号)。
(2)若上述关系中③是正确的,则溶液中的溶质为________;若上述关系中④是正确的,则溶液中的溶质为________。
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________c(NH3·H2O)(填“大于”“小于”或“等于”,下同),混合前酸中c(H+)和碱中c(OH-)的关系为c(H+)________c(OH-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了配制 100 个水分子含有 1 个钠离子的溶液,90.9 g 水中需要投入钠的质量是
A. 4.6 g B. 2.3 g C. 1.161 5 g D. 1.15 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带和海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋中提取碘的流程如下:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
某化学兴趣小组将上述流程②、③设计成如下图所示操作。

已知过程②发生反应的化学方程式为Cl2+2KI===2KCl+I2
回答下列问题:
(1)写出提取过程①、③中实验操作的名称:①____________,③____________。
(2)在灼烧过程中,使用到的实验仪器有酒精灯、____________、____________(除泥三角外)。
(3)F中下层液体的颜色为________色,上层液体中溶质的主要成分为____________。
(4)从F中得到固态碘还需进行的操作是_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】安全气囊逐渐成为汽车的标配,因为汽车发生剧烈碰撞时,安全气囊中迅速发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑,产生大量的气体使气囊迅速弹出,保障驾乘车人员安全。下列关于该反应的说法正确的是
A.该反应中NaN3是氧化剂,KNO3是还原剂
B.氧化产物与还原产物的物质的量之比为1∶15
C.若有50.5 g KNO3参加反应,则有0.5mol N原子被还原
D.每转移1 mol e,可生成标准状况下N2的体积为2.24 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr (OH)3、H2O、H2O2。 已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是______________。
(2)该反应中,发生还原反应的过程是________→________。
(3)写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目:__________。
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二元化合物X呈黑棕色晶体,易潮解,易溶于水、乙醇和乙醚;熔点306℃,沸点315℃,400℃时存在二聚体。将X加热到200℃以上释放出一种单质气体:取1.2000 g X,加热完全分解为晶体B和气体C;气体C用足量KI溶液吸收,再用0.2500 mol/L Na2S2O3溶液进行滴定,消耗29.59 mL;晶体B可溶于水,所得溶液用0.0500 mol/L的K2Cr2O7溶液进行滴定,消耗24.66 mL。设分解反应转移电子数为n,则X的摩尔质量为___________;满足条件的X是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为元素在生物体内的含量分布情况,下列表述错误的是
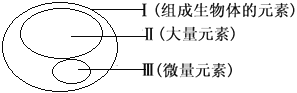
A. P、S、K、Ca、Zn属于大量元素
B. 在非生物界中都能找到,体现生物界与非生物界的统一性
C. Ⅱ和Ⅲ为生物体的必需元素,一旦缺乏就可能会导致相应的病症
D. Ⅲ含量虽少,却是生物体正常生命活动不可缺少的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入__________溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。

①A中发生反应离子方程式为_____________________。
②将仪器连接好以后,必须进行的第一步操作是_____________________。
③B装置出来的气体是否需要干燥_________________。(填“是”或“否”)
④写出装置C中发生的所有反应的化学方程式_____________,______________。
⑤D中NaOH溶液的作用_______________________。
⑥实验结束时,读取实验中生成气体的体积时,不合理的是_______________。
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为__________________。
⑧实验完成后E到F之间导管内残留水的体积会使测量结果__________。(填“偏大”、“偏小”或“不影响”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com