
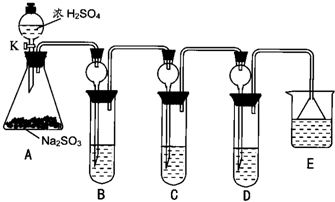
 仅用如图所示装置,检验木炭和浓硫酸反应产生的混合气体中含有的SO2和CO2.在下列表格中填写对应的药品和实验现象.
仅用如图所示装置,检验木炭和浓硫酸反应产生的混合气体中含有的SO2和CO2.在下列表格中填写对应的药品和实验现象.| 实验装置 | 检验气体 | 试剂名称 | 实验现象 |
| A | SO2 | 高锰酸钾 高锰酸钾 |
紫红色的酸性KMnO4溶液褪色 紫红色的酸性KMnO4溶液褪色 |
| B | CO2 | 氢氧化钙 氢氧化钙 |
澄清石灰水变浑浊 澄清石灰水变浑浊 |
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
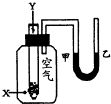 某学生用如图所示装置对化学反应:2X+Y═2Z 进行能量变化情况的研究.当往试管中加入试剂Y时,看到U型管中液面甲处上升,乙处下降.关于该反应的下列叙述:①该反应为放热反应 ②生成物的总能量比反应物的总能量高 ③该反应过程可以看成是“贮存”于X、Y内部的能量转化为热量而释放出来.其中正确的是( )
某学生用如图所示装置对化学反应:2X+Y═2Z 进行能量变化情况的研究.当往试管中加入试剂Y时,看到U型管中液面甲处上升,乙处下降.关于该反应的下列叙述:①该反应为放热反应 ②生成物的总能量比反应物的总能量高 ③该反应过程可以看成是“贮存”于X、Y内部的能量转化为热量而释放出来.其中正确的是( )| A、仅② | B、仅①③ | C、仅①② | D、仅①②③ |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
NaBr+H2SO4![]() NaHSO4+HBr
NaHSO4+HBr
CH3CH2OH+HBr![]() CH3CH2Br+H2O已知反应物的用量:NaBr(固体)0.3mol,乙醇0.25mol,浓硫酸36mL(98%,密度1.84g×cm-3),水25mL,其中乙醇的密度约为水的密度的4/5,试回答:
CH3CH2Br+H2O已知反应物的用量:NaBr(固体)0.3mol,乙醇0.25mol,浓硫酸36mL(98%,密度1.84g×cm-3),水25mL,其中乙醇的密度约为水的密度的4/5,试回答:
(1)仅用如图所示仪器安装制取和收集溴乙烷的装置,要求达到安全、损失少、不污染环境的目的,有关仪器的选择和连接顺序为(填数字)________。

(2)写出不能选用的仪器(填仪器代码,如甲、乙……)及理由。
不能选用的仪器 理由
(3)反应时,若温度过高,可见有棕色气体产生,写出反应的化学方程式:________。
(4)从棕黄色的粗溴乙烷制取无色的溴乙烷,应加入的试剂是________,必须使用的仪器是________。
(5)本实验的产率为60%,则可制取溴乙烷________g。
查看答案和解析>>
科目:高中化学 来源:志鸿系列必修一训练化学苏教版 苏教版 题型:058
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3),反应原理是
2FeSO4![]() Fe2O3+SO2↑+SO3↑.
Fe2O3+SO2↑+SO3↑.
某研究性学习小组用如图所示装置分别检验该反应所产生的气态物质,然后利用装置中A瓶内的生成物来测定已分解的FeSO4的质量.(已知:SO2沸点为-10.02 ℃,SO3的沸点为44.8℃)

请回答相关问题:
(1)A瓶所盛试剂的作用是________;B瓶所盛的试剂是________;C瓶所盛试剂的作用是________.
(2)A瓶要用冰水冷却的原因是________.
(3)将此反应生成的气体通入A瓶BaCl2溶液中,则________(填编号).
A.析出BaSO3沉淀
B.析出BaSO4沉淀
C.逸出SO3气体
D.逸出SO2气体
理由是________.
(4)反应后若用A瓶内的混合物来测定已分解的FeSO4的质量,其实验操作的第一步是(简述操作步骤)________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com