
【题目】下列有关实验操作或测量数据的说法正确的是( )
A.用托盘天平称量食盐的质量为12.35gB.中和热的测定实验中,NaOH溶液应该稍过量
C.用pH试纸测量次氯酸钠溶液的pH为11D.用碱式滴定管量取高锰酸钾溶液20.00mL
科目:高中化学 来源: 题型:
【题目】属于道尔顿近代原子论的观点有
A.原子还可由其他更小的微粒构成
B.原子中正电荷是均匀分布在整个原子中
C.原子在化学变化中保持其不可再分性
D.电子在原子核外空间做高速运动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某燃煤发电厂处理废气的装置示意图.下列说法正确的是( ) 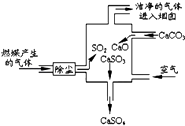
A.此过程中没有分解反应
B.整个过程的反应可表示为:2SO2+2CaCO3+O2═2CaSO4+2CO2
C.使用此废气处理装置可减少CO2的排放
D.此过程中S元素的化合价未发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用水热和有机溶剂等软化学方法,可合成出含有有机杂化锌、锗以及砷等金属的硒化物,且该硒化物具有离子交换、催化、吸附、半导体等性能,显示出良好的应用前景。回答下列问题:
(1)锌基态原子核外电子排布式为________________。元素锗与砷中,第一电离能较大的是_________(填元素符号,下同),基态原子核外未成对电子数较少的是_______________。
(2)H2SeO3分子中Se原子的杂化形式为____________,H2SeO4的酸性比H2SeO3强,原因是_________。
(3)气态SeO3分子的立体构型为____________,与SeO3互为等电子体的一种离子为_______(填离子符号)。
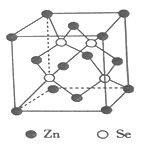
(4)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为____________,若该晶胞密度为ρg·cm-3,硒化锌的摩尔质量为Mg·mol-1。用NA代表阿伏伽德罗常数的数值,则晶胞参数ɑ为____________nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.1.0mol·L-1KNO3溶液:H+、Fe2+、Cl-、SO42-
B.能溶解Al2O3的溶液:Na+、K+、Cl-、SiO32-
C.无色透明溶液中:Al3+、Mg2+、Cl-、HCO3-
D.使甲基橙变红色的溶液:Mg2+、K+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:H2S(g)+aO2(g)===X+cH2O(l) ΔH,若ΔH表示该反应的燃烧热,则X为( )
A.S(s)B.SO2(g)C.SO3(g)D.SO3(l)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KMnO4氧化盐酸溶液.反应方程式如下:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O,若产生的Cl2在标准状况下体积为56L,
计算
(1)参加反应的HCl的物质的量?
(2)反应中被氧化的HCl的物质的量?
(3)并用双线桥标出电子转移的方向和数目.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法的目的与改变化学反应速率无关的是
A.牛奶在冰箱里保存
B.向玻璃中加入氧化铅
C.高炉炼铁前先将铁矿石粉碎
D.在糕点包装内放置小包除氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
实验编号 | HA物质的量浓度 (mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
甲 | 0.2 | 0.2 | pH=a |
乙 | c | 0.2 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明HA是强酸还是弱酸_________________________________________________。
(2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2______(选填“是”或“否”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是____________________。
(3)丙组实验结果分析,HA是________酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是________________________________。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=_____________mol·L-1。写出该混合溶液中的下列算式的精确结果 (数据不能做近似计算,不用化简)。c(Na+)-c(A-)=____________mol·L-1 c(OH-)-c(HA)=____________mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com