
分析 (1)酸或碱抑制水电离,含有弱离子的盐促进水电离,酸中氢离子或碱中氢氧根离子浓度相等时,其抑制水电离程度相等;
(2)一水合氨是弱电解质,pH=12的氨水浓度大于0.01mol/L,所以②的浓度小于③,混合后恰好完全反应,则酸的体积大于氨水;
(3)弱电解质溶液中存在电离平衡,加水稀释过程中促进弱电解质电离,相同pH的酸或碱溶液中,pH变化大的是强电解质,变化小的是弱电解质;
(4)根据溶液中氢离子和氢氧根离子浓度大小判断.
解答 解:(1)酸或碱抑制水电离,含有弱根离子的盐促进水电离,①②③④⑤抑制水电离,⑥既不促进水电离也不抑制水电离,所以水的电离程度最大的是⑥;
酸中氢离子浓度和碱中氢氧根离子浓度相等时,水的电离程度相同,②在氢离子浓度和③④中氢氧根离子浓度相等,所以水的电离程度相同的是②③④,
故答案为:⑥;②③④;
(2)一水合氨是弱电解质,pH=12的氨水浓度大于0.01mol/L,所以②的浓度小于③,混合后恰好完全反应,则酸的物质的量等于氨水的物质的量,因为酸的浓度小于氨水,所以酸的体积大于氨水,
故答案为:>;
(3)将这几种溶液稀释相同的倍数时,加水稀释促进弱电解质的电离,①中醋酸电离程度小于②,所以②中氢离子浓度大于①,所以①的pH>②;
③④中氢氧根离子浓度相等,加水稀释促进一水合氨电离,导致③中氢氧根离子浓度大于④,所以③的pH>④;
⑤中加水稀释后,促进一水合氨电离,溶液中氢氧根离子浓度减小,但溶液仍然呈碱性,⑥的混合溶液呈中性,所以pH⑤>⑥,
故答案为:>;>;>;
(4)将①、④混合,若有c(CH3COO-)>c(H+),如果溶液中c(OH-)>c(H+),则混合溶液呈碱性,如果c(HO-)<c(H+),混合溶液呈酸性,如果c(HO-)=c(H+),混合溶液呈中性,
故答案为:ABC.
点评 本题考查了弱电解质的电离及pH简单计算,题目难度中等,根据弱电解质电离特点判断相同pH的溶液中物质的量浓度关系,试题知识点较多、综合性较强,充分考查学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:解答题
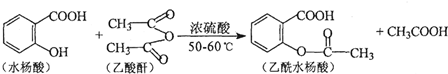
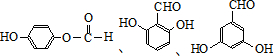 (任意一种).
(任意一种). (不写条件).
(不写条件). .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
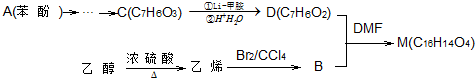
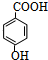 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
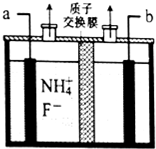 工业上通过电解含NH4F的无水熔融物生产NF3气体,其电解原理如图所示.则a极为阳极,该极的电极反应式NH4++3F--6e-=NF3+4H+,用电镀法在铁板表面镀锌或锡可防腐,这种防止金属腐蚀的方法从原理上属于覆盖保护层法.
工业上通过电解含NH4F的无水熔融物生产NF3气体,其电解原理如图所示.则a极为阳极,该极的电极反应式NH4++3F--6e-=NF3+4H+,用电镀法在铁板表面镀锌或锡可防腐,这种防止金属腐蚀的方法从原理上属于覆盖保护层法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 中学常见物质A、B、C、D、E、X,存在如图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )
中学常见物质A、B、C、D、E、X,存在如图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )| A. | 若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁 | |
| B. | 若D是一种强碱,则A、B、C均可与X反应生成D | |
| C. | 若D为NaCl,且A可与C反应生成B,则E可能是CO2 | |
| D. | 若D是一种强酸且可与铜反应生成B或C,则A既可以是单质也可以是化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 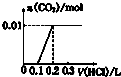 | B. | 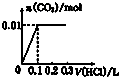 | C. | 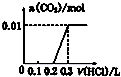 | D. | 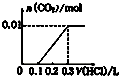 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com