
【题目】在一定条件下,可逆反应N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0。达到平衡,当单独改变下列条件后,有关叙述错误的是
2NH3(g) ΔH<0。达到平衡,当单独改变下列条件后,有关叙述错误的是
A. 加催化剂v正、v逆都发生变化,而且变化的倍数相等
B. 加压v正、v逆都增大,且v正增大的倍数大于v逆增大的倍数
C. 降温,v正、v逆都减小,且v正减小的倍数小于v逆减小的倍数
D. 加入氩气,v正、v逆都增大且v正增大的倍数大于v逆增大的倍数
【答案】D
【解析】
由反应的热化学方程式N2(g)+3H2(g)![]() 2NH3(g);△H<0可知,反应物气体的化学计量数大于生成物气体的化学计量数,增大压强,平衡向正反应方向移动;正反应放热,则升高温度平衡向逆反应方向移动。
2NH3(g);△H<0可知,反应物气体的化学计量数大于生成物气体的化学计量数,增大压强,平衡向正反应方向移动;正反应放热,则升高温度平衡向逆反应方向移动。
A项、加入催化剂,正逆反应速率都增大,且增大的倍数相同,平衡不移动,故A正确;
B项、反应物气体的化学计量数大于生成物气体的化学计量数,增大压强,v(正)、v(逆)都增大,平衡向正反应方向移动,说明v(正)增大的倍数大于v(逆)增大的倍数,故B正确;
C项、正反应放热,则升高温度平衡向逆反应方向移动,则降低温度,正逆反应速率都减小,平衡向正反应方向移动,v(正)减小的倍数小于v(逆)减小的倍数,故C正确;
D项、在体积不变的密闭容器中通入氩气,虽然压强增大,但参加反应的气体的浓度不变,反应速率不变,平衡不移动,故D错误。
故选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】最活泼的金属元素、最活泼的非金属元素、常温下呈液态的金属(价电子排布为5d106s2)元素分别位于下面元素周期表中的( )
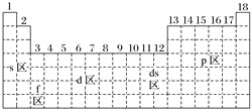
A. s区、p区、ds区 B. s区、p区、d区
C. f区、p区、ds区 D. s区、f区、ds区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝苯地平H是一种治疗高血压的药物;其一种合成路线如下:

已知:酯分子中的a-碳原子上的氢比较活泼,使酯与酯之间能发生缩合反应。
![]()
回答下列问题:
(1)B的化学名称为________.
(2)②的反应类型是________.
(3)D的结构简式为________.
(4)H的分子式为________.
(5)反应①的化学方程式为________.
(6)已知M与G互为同分异构体,M在一定条体下能发生银镜反应,核磁共振氢谱显示有4组峰,峰面积之比为1:1:2:4,写出M的一种可能的结构简式________.
(7)拉西地平 也是一种治疗高血压药物,设以乙醇和
也是一种治疗高血压药物,设以乙醇和 为原料制备拉西地平的合成路线(无机试剂任选)。________________________
为原料制备拉西地平的合成路线(无机试剂任选)。________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其化合物在人类生活、生产中发挥着重要的作用.
(1)铁是人类应用最广的金属,工业上用铁矿石(主要成分为Fe2O3 )、焦炭、石灰石在高炉中冶炼得到,高炉炼铁的主要化学反应方程式为__________________ ,其中石灰石的作用是____________________ 。
(2)铝是常见的金属,铝制容器既不能存放酸性物质,也不能存放碱性物质,其原因分别用离子方程式表示:_____________、 _____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定质量的NaBr、NaI的混合物平均分成四等份,分别加水配成溶液并编号甲、乙、丙、丁。再分别向各溶液中通入一定体积的氯气。将反应后所得溶液蒸干、灼烧的固体质量列表如下:
编号 | 甲 | 乙 | 丙 | 丁 |
固体成分 | NaCl、NaBr、NaI | NaCl、NaBr、NaI | NaCl、NaBr | NaCl |
Cl2体积/mL | V | 2V | 3V | 4V |
固体质量/g | 77.3 | 59.0 | 45.4 | 40.95 |
(1)在标准状况下,Cl2的体积V为___________mL。
(2)原混合物中NaBr的物质的量为__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有反应CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下
A. 加入催化剂,改变了反应的途径,反应的ΔH也随之改变
B. 改变压强,平衡不发生移动,反应放出的热量不变
C. 升高温度,反应速率加快,反应放出的热量不变
D. 增大反应物浓度,反应的ΔH也随之改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置(气密性已检查)制备Fe(OH)2白色沉淀。

请回答:
(1) 仪器1的名称________。装置5的作用________。
(2) 实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使溶液能进入4中________。
(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:

相关金属离子[c0(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式____________________________________________________。
(2)“氧化”中添加适量的MnO2的作用是将________________________。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_____________________________________________________________________。
(6)写出“沉锰”的离子方程式___________________________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMn![]() 时,z=___________。
时,z=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温恒容的密闭容器中充入浓度均为1 mol/L的NH3和HCl,发生NH3(g) + HCl(g)![]() NH4Cl(?) △H = -a kJ/mol,下列说法正确的是
NH4Cl(?) △H = -a kJ/mol,下列说法正确的是
A. 现象为产生白雾
B. 反应物的活化能为a kJ/mol
C. 该条件下,混合气体的平均摩尔质量始终不变
D. 任何温度下,该反应均能自发进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com