
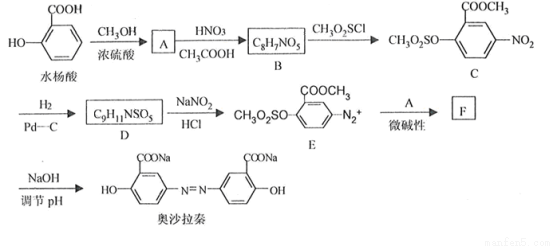
����ѧ����ѡ��5���л���ѧ��������ɳ�������ֿ���ҩ����ϳ�·�����£�
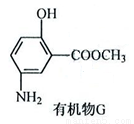
��֪����NaNO2����ǿ������
 ��
��
��1��ˮ���������������ŵ�������___________��
��2��A�ķ���ʽ��___________��
��3��B��C�Ļ�ѧ����ʽ___________��
��4�������ϳ�·�߿������B��C�����������___________��
��5��D�Ľṹ��ʽ��___________��D��E�ķ�Ӧ������___________��
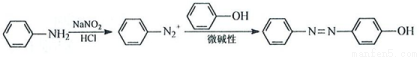
��6���л���G���ṹ��ʽ������ͼ��Ҳ�����ںϳɰ�ɳ���ء�����һ��ͬ���칹��X�Ǧ�-�����ᣬ����FeCl3��Һ������ɫ��Ӧ�������Ľṹ��_____�֣�д��һ��X���ܵĽṹ��ʽ________��
 �㽭��У��ʦ���ϵ�д�
�㽭��У��ʦ���ϵ�д� ȫ�ų��100��ϵ�д�
ȫ�ų��100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������������и߶������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�л�����ҩ���������м��壬��ṹ��ʽ����ͼ��
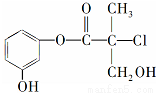
�����й���������ȷ����( )
A�����л�����Ũ��ˮ�ɷ���ȡ����Ӧ
B�����л�����Ũ�����Ϲ��ȿɷ�����ȥ��Ӧ
C��1mol���л���������NaOH��Һ��Ӧ�������4molNaOH
D�����л��ᆳ��������������������ͭ����Һ��������ש��ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭������һ�и߶��µڶ��ζο���ѧ�Ծ��������棩 ���ͣ�ѡ����
һ��-C3H7��һ��-C3H7Oȡ�������ϵ���ԭ�ӣ��γɵ��л�������������Ʒ�Ӧ��ͬ���칹����(�����������칹)
A��18�� B��24�� C��30�� D��36��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������и߶������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
ԭ��Cr2O72-+CH3CH2OH+H++H2O [Cr(H2O)6]3++CH3COOH(δ��ƽ)�����ڼ��˾���Ƿ�ƺ��ʻ������˵����ȷ����
[Cr(H2O)6]3++CH3COOH(δ��ƽ)�����ڼ��˾���Ƿ�ƺ��ʻ������˵����ȷ����
A������1molCH3CH2OHʱת�Ƶ��ӵ����ʵ���Ϊ4mol
B��1mol/LCH3COOH��Һ�к��Цļ�����ĿΪ7NA
C��H2F+��NH2-��H2S��CH4����H2O��Ϊ�ȵ�����
D���������[Cr(H2O)6]3+�У�H��Oԭ������������Cr3+�γ���λ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������и߶������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������ȷ����
A��Ӳ���ɴ�С�����ʯ��̼���裾�����
B���۵��ɸߵ��ͣ�SiC��Si��SiO2��Ge
C���е��ɸߵ��ͣ�NH3��PH3��AsH3��SbH3
D���������ɴ�С��NaI��NaBr��NaCl��NaF
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ�����µ��Ĵ�ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���á�
��1���ڹ̶�������ܱ������У��������»�ѧ��Ӧ�� N2(g)+3H2(g)  2NH3(g)
2NH3(g) 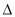 H=-92.4 kJ/mol����ƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
H=-92.4 kJ/mol����ƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
T/K | 298 | 398 | 498 |
ƽ�ⳣ��K | 4.1��106 | K1 | K2 |
�����ж�K1 K2����д��>����=����<������
������ϳɰ���Ӧ�ķ���ʽдΪ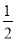 N2(g)+
N2(g)+  H2(g)
H2(g) NH3(g)����ƽ�ⳣ��ΪK������K����K�Ĺ�ϵΪ_________������ĸ��
NH3(g)����ƽ�ⳣ��ΪK������K����K�Ĺ�ϵΪ_________������ĸ��
A��K�� = K B.K�� = 2K C. K�� = 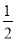 K D.K�� =
K D.K�� = 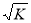
��2�����и�����˵���ϳɰ���Ӧ�Ѵﵽƽ��״̬���� ������ĸ������Ӧ���ڹ̶�������ܱ������н��еģ�
a��������N2��H2��NH3��Ũ��֮��Ϊ1��3��2 b��v(N2)(��) = 3v(H2)(��)
c��������ѹǿ���ֲ��� d�����������ܶȱ��ֲ���
e����������ƽ��Ħ����������
��3����0��3 mol N2��0��5 mol H2�������������ܱ������У���һ�������´ﵽƽ�⣬�������������ѹǿ��Ϊԭ����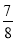 ����ʱH2��ת����Ϊ ������߸�������H2��ת���ʣ����д�ʩ���е��� (��ѡ����ĸ)��
����ʱH2��ת����Ϊ ������߸�������H2��ת���ʣ����д�ʩ���е��� (��ѡ����ĸ)��
A���������а�ԭ�����ٳ���ԭ���� B�����������ٳ���һ����H2
C���ı䷴Ӧ�Ĵ��� D��Һ��������������
��4�������£�N2H6Cl2����һ����Ҫ�Ļ���ԭ�ϣ��������ӻ����������ˮ����Һ�����ԣ�ˮ��ԭ����NH4Cl���ơ�
��д�������µ�һ��ˮ�ⷴӦ�����ӷ���ʽ ��
��������ˮ��Һ������Ũ�ȵ�����˳����ȷ���� ������ţ���
A��c(Cl��)>c(N2H62+)>c(H+)>c(OH��)
B��c(Cl��)>c([N2H5��H2O+])> c(H+)>c(OH��)
C��2 c(N2H62+)+ c([N2H5��H2O] +)= c(H+)+c(OH��)
D��c(N2H62+)> c(Cl��)>c(H+)>c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ�����µ��Ĵ�ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ����ᡢ���������ϵ�㷺������˵����ȷ���ǣ� ��
A��������ش���ˮ��ԭ����������ȫ��ͬ
B���ƹ�ú��������Һ���������ܼ��ٶ�����̼���ŷ�
C�����������������ڽ��ػ����������������ָ��������������ǽ�������
D��ʳƷ��ȫ�����������Ӽ�����������ӵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ����ģ��Ѻ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
�״���һ������ȼ�ϣ��ڹ�ҵ�ϳ���CO��H2�ϳɼ״�����Ӧ����ʽΪCO(g)+2H2(g)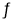 CH3OH(g)��
CH3OH(g)��
��֪��
��CO(g)��1/2O2(g)��CO2(g) ��H1����283.0kJ/mol
��H2(g)��1/2O2(g)��H2O(g) ��H2����241.8kJ/mol
��CH3OH(g)��3/2O2(g)��CO2(g)��2H2O(g) ��H3����192.2kJ/mol
�ش��������⣺
��1������CO(g)+2H2(g)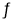 CH3OH(g)�ķ�Ӧ�ȡ�H4=____________��
CH3OH(g)�ķ�Ӧ�ȡ�H4=____________��
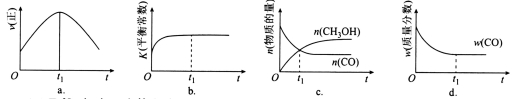
��2�����ھ��ȡ����ݵ��ܱ������г���1 mol CO��2 mol H2������CO(g)+2H2(g)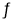 CH3OH(g)��Ӧ������ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ��Ϊƽ��״̬����________(��ѡ����ĸ)��
CH3OH(g)��Ӧ������ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ��Ϊƽ��״̬����________(��ѡ����ĸ)��
��3��T1��ʱ����һ�����Ϊ5 L�ĺ��������г���1 mol CO��2 mol H2������5 min�ﵽƽ�⣬CO��ת����Ϊ0.8����5 min����H2��ʾ�ķ�Ӧ����Ϊv(H2)=_______��T1��ʱ������һ���������ܱ�������Ҳ����1 mol CO��2 mol H2���ﵽƽ��ʱCO��ת����Ϊ0.7��������������____5 L(�>����<����=��)��T1��ʱ��CO(g)+2H2(g)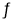 CH3OH(g)��ƽ�ⳣ��K=______________��
CH3OH(g)��ƽ�ⳣ��K=______________��
��4����T1��ʱ�������Ϊ5 L�ĺ��������г���һ������H2��CO����Ӧ�ﵽƽ��ʱCH3OH�����������n(H2)��n(CO)�Ĺ�ϵ��ͼ��ʾ���¶Ȳ��䣬�� ʱ���ﵽƽ��״̬��CH3OH���������������ͼ���е�______�㡣
ʱ���ﵽƽ��״̬��CH3OH���������������ͼ���е�______�㡣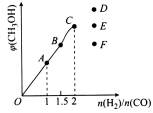
��5��Ϊ�����ȼ�ϵ������ʿ��Խ��״����Ϊȼ�ϵ�أ�д��KOH���������Һʱ���״�ȼ�ϵ�صĸ�����Ӧʽ��___________________���õ�ظ�����ˮ�����բ����ʱ�����Ա�����բ������ʴ�����ֵ绯ѧ������������___________��
��6�����м״��ķ�ˮ�����ŷŻ����ˮ��Ⱦ������ClO2��������ΪCO2��Ȼ���ټӼ��кͼ��ɡ�д�������״����Է�ˮ�����У�ClO2��״���Ӧ�����ӷ���ʽ��___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ��һƽ�а������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и������ʵıȽ�����ȷ���ǣ� ��
A������HClO4��HBrO4��HIO4
B������Ba(OH)2��Ca(OH)2��Mg(OH)2
C���ȶ���HCl��PH3��H2S
D����ԭ��Cl-��Br-��I-
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com