
【题目】

(1)该硫酸的物质的量浓度为________________;
(2)实验室用该硫酸配制240mL0.46 mol·L-1的稀硫酸,则
① 需要该硫酸的体积为________mL;
② 有以下仪器: A 烧杯 B 100mL量筒 C 250mL容量瓶
D 500mL容量瓶 E 玻璃棒 F 托盘天平(带砝码)
G 10mL量筒 H 胶头滴管。配制时,必须使用的仪器有______________(填代号);
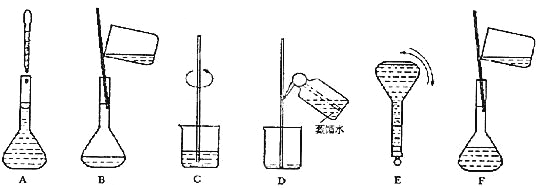
![]() ③ 配制过程中有几个关键的步骤和操作如下图所示:将上述实验步骤A—F按实验过程先后次序排列。
③ 配制过程中有几个关键的步骤和操作如下图所示:将上述实验步骤A—F按实验过程先后次序排列。
④ 该同学实际配制得到的浓度为0.45 mol·L-1,可能的原因是_________
A.量取浓H2SO4时仰视刻度 | B.容量瓶洗净后未经干燥处理 |
C.没有将洗涤液转入容量瓶 | D.定容时仰视刻度 |
【答案】(1)18.4mol/L
(2)①6.3②A C E G H(多选错选不给分,少写1或2个给1分)
③C B D F A E④C D
【解析】试题分析:(1)根据题给信息知该硫酸的密度为1.84g/cm3,质量分数为98%,根据公式c=![]() 计算该该硫酸的物质的量浓度为18.4mol/L ;
计算该该硫酸的物质的量浓度为18.4mol/L ;
(2)①配制240mL0.46 mol·L-1的稀硫酸需用250mL的容量瓶,根据公式c1V1=c2V2计算V2= c1V1/c2=(250×0.46)/18.4=6.3mL;②该实验的实验步骤为:计算、称量、溶解并却、转移、洗涤、定容、摇匀。根据实验步骤确定实验仪器。配制时,必须使用的仪器有ACEGH;③该实验的实验步骤为:计算、称量、溶解并却、转移、洗涤、定容、摇匀。实验步骤按实验过程先后次序排列为CBDFAE。
④ A、量取浓H2SO4时仰视刻度,量取的浓硫酸体积偏大,所配溶液的浓度偏高,错误;B、容量瓶洗净后未经干燥处理,对所配溶液的浓度无影响,错误;C、没有将洗涤液转入容量瓶,溶质损失,所配溶液的浓度偏低,正确;D、定容时仰视刻度,所配溶液的体积偏大,浓度偏低,正确,选CD。


科目:高中化学 来源: 题型:
【题目】冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或氢气或一氧化碳)法;③活泼金属置换法;④电解法。四种方法在工业上均有应用,古代有(1)火烧孔雀石炼铜;(2)湿法炼铜;现代有(3)铝热法炼铬;(4)从光卤石(KCl·MgCl2·6H2O)中炼镁。对它们的冶炼方法的分析不正确的是( )
A.(1)用①B.(2)用②C.(3)用③D.(4)用④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子RO4n-中共有x个核外电子,R原子的质量数为A,则R原子核内含中子的数目
A.A+n+32-xB.A+n-24-xC.A-n+24-xD.A+n+24-x
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水解离子方程式表达正确的是( )
A.CH3COONa的溶液:CH3COO﹣+H2O═CH3COOH+OH﹣
B.NH4Cl的溶液:NH ![]() +H2O?NH3?H2O+H+
+H2O?NH3?H2O+H+
C.Na2CO3的溶液:CO ![]() +H2O?H2CO3+2OH﹣
+H2O?H2CO3+2OH﹣
D.AlCl3的溶液:Al3++3H2O═Al(OH)3↓+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.0.1 mol?L﹣1的醋酸加水稀释, ![]() 减小
减小
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大
C.体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少
D.常温下,pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合,溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
①燃料电池的反应物可不储存在电池的内部
②锌锰干电池是一次电池,铅蓄电池是二次电池
③锂电池是新一代可充电电池
④燃料电池作为汽车驱动能源已研发成功
A.②③④B.①②③④
C.①②③D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学工作者一直关注食品安全,发现有人将工业染料“苏丹红1号”非法用作食用色素.苏丹红是一系列人工合成染料,其中“苏丹红4号”的结构式如图:  下列关于“苏丹红4号”说法正确的是( )
下列关于“苏丹红4号”说法正确的是( )
A.不能发生加成反应
B.属于甲苯同系物
C.属于芳香烃
D.能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol/LNaHC2O4溶液中滴加0.01 mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是
A. V(NaOH)=0时,c(H+)=1×10-2mol/L
B. V(NaOH)<10mL时,不可能存在c(Na+)=2c(C2O42-)+c(HC2O4-)
C. V(NaOH)=10mL时,c(H+)=1×10-7mol/L
D. V(NaOH)>10mL时,c(Na+)>c(C2O42-)>c(HC2O4-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com