
| A、白磷分子呈正四面体,键角109°28′,1mol白磷含共价键6mol |
| B、臭氧分子呈直线型,等质量的臭氧和氧气所含的氧原子数相同 |
| C、S8是分子晶体,8个硫原子在同一个平面上,摩尔质量为256g |
| D、石墨晶体呈层状结构,每个碳原子只有3个价电子形成共价键 |
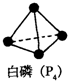 ,白磷分子呈正四面体,键角60°,1mol白磷含共价键6mol,故A错误;
,白磷分子呈正四面体,键角60°,1mol白磷含共价键6mol,故A错误;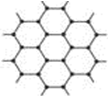 ,每个碳原子与其它3个碳原子形成3个共价键,所以每个碳原子只有3个价电子形成共价键,故D正确;
,每个碳原子与其它3个碳原子形成3个共价键,所以每个碳原子只有3个价电子形成共价键,故D正确;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.下列说法正确的是( )
工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.下列说法正确的是( )| A、曲线Ⅱ对应的条件改变是降低压强 |
| B、若曲线I对应的条件改变是升高温度,则该反应△H>0 |
| C、反应开始至a点时v(H2)=1mol?L-1?min-1 |
| D、其它条件不变,若降低该反应的温度,平衡常数值将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2O+O2+4e-═4OH- |
| B、Fe-3e-═Fe3+ |
| C、Fe2++2OH-═Fe(OH)2 |
| D、4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,46g NO2中含有氧原子个数为2NA |
| B、在标准状况下,22.4 L丙烷中所含C-H键数目为6NA |
| C、将58.5g NaCl溶于1 L水中,溶液中所含Na+和Cl-总数为2NA |
| D、以二氧化锰和浓盐酸为原料制备氯气,当生成1mol氯气,电子转移总数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
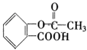 )具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药.写出阿司匹林与足量NaOH溶液共热反应的化学方程式:
)具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药.写出阿司匹林与足量NaOH溶液共热反应的化学方程式: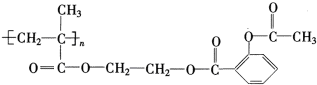
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下浓H2SO4能使铝发生钝化,可在常温下用铝制容器贮运浓硫酸 |
| B、Cl2能与石灰乳反应,可用于制取漂白粉 |
| C、二氧化氯具有氧化性,可用于自来水的杀菌消毒 |
| D、石墨具有导电性,可用于制造半导体材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com