
下图所示是可逆反应A+2B![]() 2C+3D的化学反应速率和化学平衡随外界条件改变而变化的情况:
2C+3D的化学反应速率和化学平衡随外界条件改变而变化的情况:
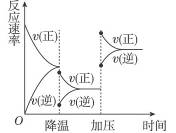
由图可判断:
(1)正反应是_____________(吸热、放热)反应。
(2)若A、B是气体,则C的状态是__________,D的状态是______________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:高中化学习题 题型:022
在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧分别进行如下图所示的可逆反应.
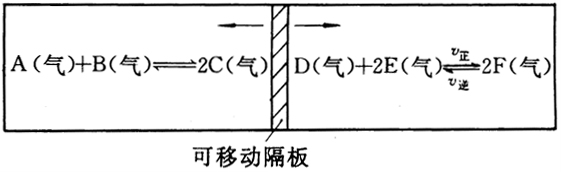
各物质的起始加入量如下:A、B和C均为4.0mol,D为6.5mol,F为2.0mol,设E为![]() .当
.当![]() 在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器的正中位置.请填写以下空白:
在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器的正中位置.请填写以下空白:
(1)若![]() ,则右侧反应在起始时向________(填“正反应”或“逆反应”)方向进行.欲使起始反应维持向该方向进行,则
,则右侧反应在起始时向________(填“正反应”或“逆反应”)方向进行.欲使起始反应维持向该方向进行,则![]() 的最大取值应小于________.
的最大取值应小于________.
(2)若![]() 分别为4.5和5.0,则在这两种情况下,当反应达平衡时,A的物质的量是否相等?________(填“相等”“不相等”或“不能确定”).其理由是________.
分别为4.5和5.0,则在这两种情况下,当反应达平衡时,A的物质的量是否相等?________(填“相等”“不相等”或“不能确定”).其理由是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
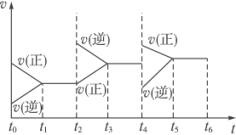
(1)处于平衡状态的时间段有____________。
(2)起始时投入的物质成分为____________。
A.SO2,O2
B.SO2,SO3
C.SO3
D.SO2,O2,SO3
(3)t2—t3、t4—t5时间段平衡的移动方向分别为____________、____________。(填“正反应方向”或“逆反应方向”)
查看答案和解析>>
科目:高中化学 来源: 题型:
在一恒容密封容器中发生可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下图所示是某一段时间内反应速率与反应进程的曲线关系图。完成下列问题:
2SO3(g),下图所示是某一段时间内反应速率与反应进程的曲线关系图。完成下列问题:
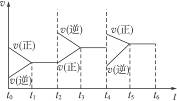
(1)处于平衡状态的时间段有____________。
(2)起始时投入的物质成分为____________。
A.SO2,O2 B.SO2,SO3
C.SO3 D.SO2,O2,SO3
(3)t2—t3、t4—t5时间段平衡的移动方向分别为____________、____________。(填“正反应方向”或“逆反应方向”)
查看答案和解析>>
科目:高中化学 来源: 题型:
目前常用的镍-镉电池的电池反应式可以表示为:
2Ni(OH)2+Cd(OH)2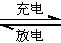 Cd+2NiO(OH)+2H2O
Cd+2NiO(OH)+2H2O
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸。
试回答以下问题:
(1)该反应_______(填“是”或“不是”)可逆反应。
(2)废弃的镍-镉电池已成为重要的环境污染物,有资料表明一节废镍-镉电池可以使一平方米面积的耕地失去使用价值,在酸性土壤中这种污染尤为严重,这是因为____________________。
(3)下图所示是废镍-镉电池中的重金属离子渗入水体后,又进入人体的一条途径:
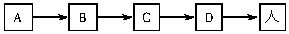
生物体D中重金属离子的浓度___________(填“大于”、“等于”或“小于”)生物体A中的浓度,这是通过食物链___________作用所引起的,除上述途径外,被污染水体中的重金属离子还可以直接通过__________(填途径)进入人体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com