

分析 该反应为气体体积减小、放热的反应,由图可知,t0~t1为原平衡,t1~t2时正逆反应速率均增大,且平衡逆向移动,则改变条件为升高温度;t3~t4时正逆反应速率均增大,且平衡不移动;t4~t5时正逆反应速率均减小,且平衡逆向移动,则改变条件为减小压强,平衡逆向移动导致C的百分含量减小,则t0~t1时C的百分含量最高,以此来解答.
解答 解:(1)由上述分析可知,改变条件分别为t1为升高温度;t4 为减小压强,
故答案为:升高温度;减小压强;
(2)t0~t1为原平衡,t2~t3时平衡逆向移动,t3~t4时平衡不移动;t4~t5时平衡逆向移动,平衡逆向移动导致A的体积分数变大,则t5~t6时A的体积分数最大,
故答案为:t5~t6;
(3)由图可知,纵坐标为反应速率,则反应速率最大的时间段是t3~t4,
故答案为:t3~t4;
(4)K与温度有关,该反应为放热反应,升高温度平衡逆向移动导致K减小,则t1为升高温度,其它时间段温度不变,则K0>K3=K5,
故答案为:K0>K3=K5.
点评 本题考查化学平衡移动、化学反应速率及平衡的图象,为高频考点,把握温度、浓度、压强对平衡移动及速率的影响为解答本题关键,侧重分析与应用能力的考查,注意速率与平衡移动的关系,(4)为解答的难点,题目难度不大.


 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下不能用铝制容器贮存 | |
| B. | 露置在空气中,容器内酸液的质量都增加 | |
| C. | 露置在空气中,容器内酸液的浓度都减小 | |
| D. | 常温下都能与铜剧烈反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采取低碳、节俭的生活方式 | |
| B. | 按照规定对生活废弃物进行分类放置 | |
| C. | 深入农村和社区宣传环保知识 | |
| D. | 绿色化学的核心是应用化学原理治理环境污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏法是海水淡化的主要方法之一 | |
| B. | 工业用电解氧化镁的方法制取金属镁 | |
| C. | 用氯气将苦卤中的溴离子氧化以提取溴 | |
| D. | 用石灰从海水中“沉镁”得到氢氧化镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | A分子属于酯类化合物,在一定条件下能发生水解反应 | |
| B. | A在一定条件下可与3molH2发生加成反应 | |
| C. | 符合题中A分子结构特征的有机物只有一种 | |
| D. | 与A属于同类化合物的同分异构体只有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 反应A(g)?B(g)+C(g)在容积为1.0L的密闭容器中 进行,A的初始浓度为0.050mol/L.温度T1和T2下A的浓度与时间关系如图所示.回答下列问题:
反应A(g)?B(g)+C(g)在容积为1.0L的密闭容器中 进行,A的初始浓度为0.050mol/L.温度T1和T2下A的浓度与时间关系如图所示.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 是一种有机烯醚,可以用烃A通过下列路线获得A$→_{①}^{Br_{2}/CCl}$B$→_{②}^{NaOH水溶液/△}$C$→_{③}^{浓H_{2}SO_{4}/△}$
是一种有机烯醚,可以用烃A通过下列路线获得A$→_{①}^{Br_{2}/CCl}$B$→_{②}^{NaOH水溶液/△}$C$→_{③}^{浓H_{2}SO_{4}/△}$
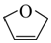 的同分异构体的结构简式(写出2种)HC≡CCH2CH2OH、CH3C≡CCH2OH
的同分异构体的结构简式(写出2种)HC≡CCH2CH2OH、CH3C≡CCH2OH查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com