
【题目】将一定量的铝粉、氧化铝、氧化镁的混合物加入到300mL4mol/L的稀硫酸中,生成标准状况下6.72L气体。向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,所得沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系如图所示:
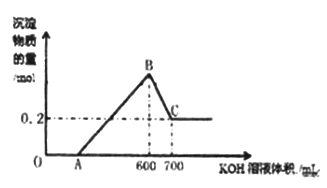
(1)OA对应反应的离子方程式为________________,BC对应反应的离子方程式为_________________;
(2)c(KOH)=_________mol/L,混合物中氧化铝的物质的量为_____mol;
(3)A点对应的数值为_______;
(4)在中学阶段,实验室里检验B点对应的溶液中的阳离子时,所观察到的现象是___________。
(5)向C点对应的溶液中通入足量的CO2所发生反应的离子方程式为__________________。
【答案】 H+ +OH-=H2O Al(OH)3 +OH-=AlO2-+2H2O 4 0.1 200 透过蓝色钴玻璃观察,火焰呈紫色 CO2 +AlO2- +2H2O=Al(OH)3↓+HCO3-
【解析】将一定量的铝粉、氧化铝、氧化镁的混合物加入到300mL4mol/L的稀硫酸中,生成标准状况下6.72L气体,氢气的物质的量为![]() 0.3mol,根据2Al~~3H2,混合中Al粉的物质的量为0.3mol×
0.3mol,根据2Al~~3H2,混合中Al粉的物质的量为0.3mol×![]() =0.2mol;向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,根据沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系图,可知:(1)OA段酸过量,发生酸碱中和反应,离子反应方程式为H+ +OH-=H2O;继续滴加KOH溶液将溶液里的Al3+和Mg2+转化为Al(OH)3和Mg(OH)2沉淀,BC段滴加KOH溶液,溶解生成的Al(OH)3沉淀,发生反应的离子方程式为Al(OH)3 +OH-=AlO2-+2H2O;
=0.2mol;向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,根据沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系图,可知:(1)OA段酸过量,发生酸碱中和反应,离子反应方程式为H+ +OH-=H2O;继续滴加KOH溶液将溶液里的Al3+和Mg2+转化为Al(OH)3和Mg(OH)2沉淀,BC段滴加KOH溶液,溶解生成的Al(OH)3沉淀,发生反应的离子方程式为Al(OH)3 +OH-=AlO2-+2H2O;
(2)B点为完全沉淀点,此时溶液中溶质K2SO4,根据原子守恒可知n(K+)=2n(SO42-)=2×0.3L×4mol/L=2.4mol,此时消耗KOH溶液体积为0.6L,则c(KOH)=![]() =4mol/L;BC段共消耗KOH溶液体积为0.1L,根据Al(OH)3 +OH-=AlO2-+2H2O可知Al(OH)3 的物质的量为4mol/L×0.1L=0.4mol;设氧化铝的物质的量为n mol,根据原子守恒2n mol+0.2 mol=0.4mol,n=0.1;
=4mol/L;BC段共消耗KOH溶液体积为0.1L,根据Al(OH)3 +OH-=AlO2-+2H2O可知Al(OH)3 的物质的量为4mol/L×0.1L=0.4mol;设氧化铝的物质的量为n mol,根据原子守恒2n mol+0.2 mol=0.4mol,n=0.1;
(3)C点对应的沉淀Mg(OH)2物质的量为 0.2mol,则生成沉淀Mg(OH)2和Al(OH)3 消耗KOH的物质的量为0.2mol×2+0.4mol×3=1.6mol,消耗KOH溶液的体积为![]() =400mL,则A点对应的数值为600mL-400mL=200mL;
=400mL,则A点对应的数值为600mL-400mL=200mL;
(4)K+的检验可用焰色反应,具体操作是透过蓝色钴玻璃观察,火焰呈紫色;
(5)C点对应的溶液中含有AlO2-,通入足量的CO2所发生反应的离子方程式为CO2 +AlO2- +2H2O=Al(OH)3↓+HCO3-;


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】在Na+浓度为0.5 mol/L的某澄清溶液中,还可能含有下表中的若干种离子。
阳离子 | K+、Ag+、Mg2+、Ba2+ |
阴离子 | NO3-、CO32-、SiO32-、SO42- |
已知:(1)SiO32-和大量的H+会生成白色沉淀H2SiO3;
(2)H2SiO3![]() H2O+SiO2;
H2O+SiO2;
(3)产生气体为在标准状况下测定,不考虑气体在水中的溶解。现取该溶液100 mL进行如下实验:
序号 | 实验内容 | 实验结果 |
Ⅰ | 向该溶液中加入足量稀盐酸 | 产生白色沉淀并放出0.56 L气体 |
Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4 g |
Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
请回答下列问题:
(1)实验Ⅰ能确定一定不存在的离子是______________________。
(2)实验Ⅰ中生成沉淀的离子方程式为______________________。
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)。
阴离子 | NO3- | CO32- | SiO32- | SO42- |
c/mol·L-1 | ______ |
(4)判断K+是否存在,若存在求其最小浓度,若不存在说明理由:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在溶液中大量共存的是( )
A.H+、Ca2+、NO3-、CO32-B.K+、Na+、Br-、NO3-
C.Ag+、Na+、Cl-、K+D.NH4+、K+、NO3-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:O2(g)+2H2(g)=2H2O(g)△H=﹣483.6kJmol﹣1
C(s,石墨)+O2(g)=CO2(g)△H=﹣393.5kJmol﹣1
CO2(g)+C(s,石墨)=2CO(g)△H=+172.5kJmol﹣1
(1)请写出CO与水蒸汽反应的热化学方程式
(2)在一体积为10L的密闭容器中,通入一定量的CO和水蒸汽,在850℃时发生反应,容器中CO和水蒸汽浓度变化如图,则0~4min的平均反应速率v(CO)= , 请计算此时的平衡常数K= . 
时间/min | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表.
①表中3min~4min之间反应处于状态;c1数值0.08mol/L (填大于、小于或等于).
②反应在4min~5min间,平衡向逆方向移动,可能是以下的原因(填字母),表中5min~6min之间数值发生变化,可能的原因是 . (填字母)
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 含有氧元素的化合物一定是氧化物
B. 纯净物一定由同种分子构成
C. 含一种元素的物质一定是单质
D. 由同种分子构成的物质一定是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子化合物用碘蒸气处理后,其导电能力大幅提高。上述高分子化合物的单体是
A.乙炔B.乙烯C.丙烯D.1,3-丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,互为同分异构体的是:
A. 金刚石和足球烯(C60)
B. 尿素[(NH2)2CO] 和氰酸铵(NH4CNO)
C. H2O和D2O
D. 苯和甲苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com