
| A. | 化学反应过程中,一定有化学键的断裂和形成 | |
| B. | 日常生活中的废旧电池会污染环境,所以应集中填埋处理 | |
| C. | 化学反应过程中,分子的种类和数目一定发生改变 | |
| D. | 放热反应的反应速率,一定比吸热反应的反应速率快 |
分析 A.化学反应过程中反应物要断键、生成新物质要成键;
B.电池中的重金属等污染土壤和水体;
C.化学反应中分子种类发生变化,但是分子数目可能不变;
D.反应速率快慢与吸热反应、放热反应无关.
解答 解:A.化学反应的过程实际上是旧键断裂、新键生成的过程,故A正确;
B.电池中的重金属等污染土壤和水体,所以废旧电池应集中回收,但不能填埋处理,故B错误;
C.化学反应过程中有新物质生成,则反应中分子种类发生变化,而分子的数目不一定变化,故C错误;
D.反应速率的大小与反应的类型无关,放热反应的反应速率不一定比吸热反应的反应速率大,故D错误;
故选A.
点评 本题考查较为综合,涉及反应热与焓变、化学反应速率的影响因素、常见污染物治理等知识,题目难度不大,明确化学反应实质为解答关键,D为易错点,注意反应速率与反应类型没有必然关系.


科目:高中化学 来源: 题型:解答题
| 实验目的 | 试剂及方法 |
| 证明炭粉中含有CuO | |
| 鉴别MgCl2和AlCl3溶液 | |
| 分离Na2SO4和CaCO3固体混合物 | |
| 除去NaHCO3溶液中混有的Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
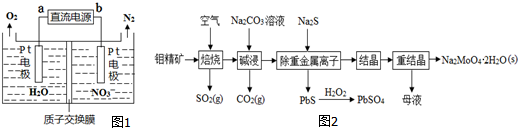
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
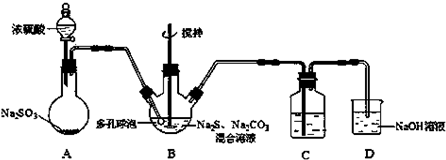
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=+890.3 kJ•mol-1 | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-890.3 kJ•mol-1 | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-890.3 kJ | |
| D. | 2H2(g)+O2(g)═2H2O(l);△H=-285.8 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
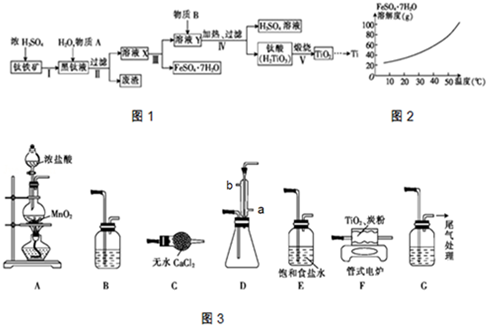
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气质量等级为优 | |
| B. | 二氧化硫的污染指数可能为42 | |
| C. | 目前,我国大部分地区空气中二氧化硫、二氧化氮及可吸入颗粒物等物质的含量偏高 | |
| D. | 对煤、石油等燃料进行脱硫处理、使用氢气等清洁燃料、通过静电沉降器除去悬浮颗粒物都可以治理大气污染,改善空气质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com