
| 实验装置 | 电解质溶液 | 实验现象 | |
 | 5mol/L NaCl溶液 | a极附近 | b极附近 |
| 开始时,产生白色浑浊并逐渐增加,当沉入U形管底部时部分沉淀变为橙黄色;随后a极附近沉淀自下而上也变为橙黄色 | 产生无色气泡 | ||
| ①氯化亚铜(CuCl)为白色粉末,微溶于水; ②氢氧化亚铜(CuOH)为黄色不溶于水的固体,易脱水分解为红色的Cu2O; ③Cu+水溶液中不稳定,酸性条件下易歧化为Cu2+和Cu; ④氢氧化铜可以溶于浓NaOH得到蓝色溶液. |
分析 (1)电解池阳极发生氧化反应,阴极发生还原反应,依据题意b极产生的气体是H2,则b极氢离子得到电子发生还原反应;
(2)依据(1)可知a极为阳极,铜做阳极为活性电极,结合a极附近生成的白色浑浊是CuCl写出电极反应式;
(3)用铜电极电解饱和食盐水时,阳极发生氧化反应,电极反应为Cu-e-+Cl-=CuCl,阴极发生还原反应,电极方程式为2H++2e-=H2↑,开始时生成CuCl白色生成,随着反应进行,溶液pH逐渐增大,因Kap(CuOH)<Kap(CuCl),则可生成CuOH橙黄色沉淀,CuOH不稳定分解生成Cu2O和水;
(4)氧化亚铜与稀硫酸反应生成铜单质、铜离子和水;
(5)用Cu电极电解5mol/L NaOH溶液,实验时观察到阳极产生大量无色气泡为氧气,氧气具有强的氧化性,能够氧化CuOH,据此解答.
解答 解:(1)用铜做电极,电解氯化钠溶液,b极产生的气体是H2,则b极氢离子得到电子发生还原反应,为阴极,电极反应式为:2H2O+2e-=H2↑+2OH-,因为b极生成氢氧根离子所以附近溶液pH增大;
a剂为阳极,与电源正极相连;
故答案为:增大;正;
(2)依据(1)可知a极为阳极,铜做阳极为活性电极,a极附近生成的白色浑浊是CuCl,则其电极反应式为:Cu-e-+Cl-=CuCl↓;
故答案为:Cu-e-+Cl-=CuCl↓;
(3)用铜电极电解饱和食盐水时,阳极发生氧化反应,电极反应为Cu-e-+Cl-=CuCl,阴极发生还原反应,电极方程式为2H++2e-=H2↑,开始时生成CuCl白色生成,随着反应进行,溶液pH逐渐增大,因Kap(CuOH)<Kap(CuCl),则可生成CuOH橙黄色沉淀,CuOH不稳定分解生成Cu2O和水.
①橙黄色沉淀中含有Cu2O,则CuCl转化为Cu2O的原因是,随着电解的进行,氢氧根离子浓度增大则CuCl转化为CuOH,方程式:CuCl+OH-=CuOH+Cl-,CuOH不稳定分解生成Cu2O和水,方程式:2CuOH=Cu2O+H2O,
故答案为:CuCl+OH-=CuOH+Cl-、2CuOH=Cu2O+H2O;
②通电时,在阴极产生的OH-向阳极定向移动,氢氧根离子浓度增大则CuCl转化为CuOH,而CuOH不稳定分解生成Cu2O和水,所有看到现象a极附近沉淀自下而上;
故答案为:通电时,在阴极产生的OH-向阳极定向移动;
(4)氧化亚铜与稀硫酸反应生成铜单质、铜离子和水,化学方程式:Cu2O+H2SO4=Cu+CuSO4+H2O,铜为红色固体,硫酸铜为蓝色溶液,所有现象为:沉淀溶解,溶液变蓝,且有少量红色固体产生,故答案为:沉淀溶解,溶液变蓝,且有少量红色固体产生;
(5)用Cu电极电解5mol/L NaOH溶液,实验时观察到阳极产生大量无色气泡为氧气,氧气具有强的氧化性,能够氧化CuOH,所以不能依据该现象得出“该猜想不成立”的结论;
故答案为:不能,阳极产生的大量O2可能将CuOH氧化.
点评 本题为电化学试题,考查了电解池电极反应式书写、电极现象及产物判断等,明确电解池工作原理是解题关键,注意阳极为活性电极时,电极本身参加反应,题目难度较大.


科目:高中化学 来源: 题型:选择题
| 实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| A. | 实验①中,若5min时测得n(M)=0.050mol,则0~5min时间内,用N表示的平均反应速率v(N)=l.0×10-2 mo1•L-1•min-1 | |
| B. | 实验②中,该反应的平衡常数K=2.0 | |
| C. | 实验③中,达到平衡时,X的转化率为60% | |
| D. | 该反应的正反应方向为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | |||
| Y | Z | W |
| A. | Z的最高价氧化物的水化物是强酸 | |
| B. | Y的最高价氧化物能溶于烧碱溶液 | |
| C. | X与W形成的化合物中含有离子键 | |
| D. | Z、W分别形成的简单离子中,前者的半径较大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
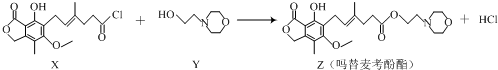
| A. | 化合物X中含有手性碳原子 | B. | 化合物Y的分子式为C6H12NO2 | ||
| C. | 1mol化合物Z可以与3mol NaOH反应 | D. | 用溴水可鉴别化合物X和Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A.天然气燃烧 | B.自然界中丁达尔效应 | C.蛋白质受热凝固 | D.食醋除水垢 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 麦芽糖及其水解产物均能发生银镜反应 | |
| B. | 饱和硫酸铵和醋酸铅溶液均能使鸡蛋清溶液发生变性 | |
| C. | 油脂、二肽发生水解反应均可能得到含羧基的物质 | |
| D. | 天然橡胶 和杜仲胶 和杜仲胶 的单体是同种物质 的单体是同种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫与氢氧化钠溶液反应 | B. | 钠与氧气的反应 | ||
| C. | 铁在硫蒸气中燃烧 | D. | 铁粉加入硝酸中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
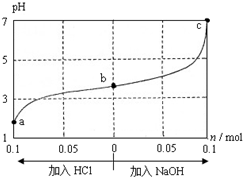 25℃时,将1.0L w mol•L-1 CH3COOH溶液与0.1mol NaOH固体混合,充分反应后向混合液中通(加)入HCl气体或NaOH固体,溶液pH随加入HCl或NaOH的物质的量而变化如图.下列叙述正确的是( )
25℃时,将1.0L w mol•L-1 CH3COOH溶液与0.1mol NaOH固体混合,充分反应后向混合液中通(加)入HCl气体或NaOH固体,溶液pH随加入HCl或NaOH的物质的量而变化如图.下列叙述正确的是( )| A. | a、b、c 对应的混合液中,水的电离程度由大到小的顺序的是a>b>c | |
| B. | c点混合液中c(Na+)>c(CH3COO-) | |
| C. | a、b、c三点都有c(CH3COO-)+c(OH-)=c(Na+)+c(H+) | |
| D. | 若忽略体积变化,则25℃时CH3COOH的电离平衡常数 K=$\frac{0.2}{w-0.2}$×10-7 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上第一次质检化学卷(解析版) 题型:选择题
下列说法正确的是
A. 某试样焰色反应呈黄色,则试样中肯定不含有K+
B. 过滤操作时,为了加快过滤可以用玻璃棒搅拌漏斗的液体
C. 蒸馏装置中,温度计水银球的位置应该在蒸馏烧瓶的支管口附近
D. 粗盐的提纯实验中,滤液在坩埚中加热蒸发结晶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com