
| A、标准状况下,22.4L HF中含有的氟原子数目为NA(NA表示阿伏加德罗常数) |
| B、0.1mol/L的NH4HSO4溶液中滴加0.1mol/L的Ba(OH)2溶液至沉淀刚好完全:c(NH4+)>c(OH-)>c(SO42-)>c(H+) |
C、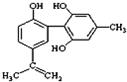 1mol如图所示物质与浓溴水反应时通常最多消耗Br2为4mol |
| D、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0,一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |


科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、医疗上的血液透析利用了胶体的性质,而土壤保肥与胶体的性质无关 |
| B、蔗糖、淀粉、油脂及其水解产物均为非电解质 |
| C、通过红外光谱分析可以区分乙醇和乙酸乙酯 |
| D、乙醇、乙酸均能与Na反应放出H2,二者分子中官能团种类相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/L氯化铜溶液中的Cu2+数小于NA |
| B、标准状况下,22.4L Cl2参加任何化学反应转移的电子数都是2NA |
| C、28 g聚乙烯含有的碳原子数为2NA |
| D、1mol CH5+所含电子数为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝溶于烧碱溶液:Al+2OH-═AlO2-+H2↑ | ||||
| B、用铜电极电解硫酸铜溶液:2Cu2++2H2O═2Cu↓+O2↑+4H+ | ||||
C、用FeCl3饱和溶液制备Fe(OH)3胶体:Fe3++3H2O(沸水)
| ||||
| D、已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色溶液.当Pb(CH3COO)2溶液中通入H2S气体时有黑色沉淀生成:Pb2++H2S═PbS↓+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配制一定物质的量浓度的溶液时,定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水到刻度 |
| B、锥形瓶盛装待测液前需先用蒸馏水洗净,再用待测液润洗 |
| C、石蕊试纸在测定气体酸碱性时必须用蒸馏水润湿 |
| D、向稀氢氧化钠溶液中滴加饱和氯化铁溶液并不断搅拌,制取氢氧化铁胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
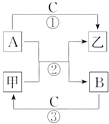 A、B、C是元素周期表中前18号元素中的3种单质,甲、乙是常见的化合物,它们之间存在如图所示关系.
A、B、C是元素周期表中前18号元素中的3种单质,甲、乙是常见的化合物,它们之间存在如图所示关系.查看答案和解析>>
科目:高中化学 来源: 题型:

| A、在蒸发皿中灼烧CuSO4?5H2O晶体以除去结晶水 |
| B、配制0.1 mol?L-1硫酸溶液时,容量瓶应先用0.1 mol?L-1硫酸溶液润洗 |
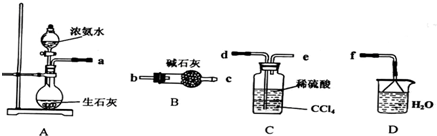
| C、用图a所示装置实验,振荡后静置,溶液不再分层,且保持无色透明 |
| D、实验室用图b所示装置制取少量的氨气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com