
| A. | N2 | B. | SO2 | C. | NH3 | D. | Cl2 |
分析 能用浓硫酸和NaOH干燥,说明该气体不和浓硫酸、NaOH反应,浓硫酸不能干燥碱性气体、部分还原性气体,氢氧化钠不能干燥酸性气体、不能干燥和它反应的部分单质.
解答 解:A.氮气属于中性气体,和浓硫酸、NaOH都不反应,所以符合条件,故A选;
B.二氧化硫属于酸性氧化物,能和NaOH反应生成钠盐,所以不能用NaOH干燥,故B不选;
C.氨气属于碱性气体,能和浓硫酸反应生成铵盐,所以不能用浓硫酸干燥,故C不选;
D.氯气能和NaOH反应生成盐,所以氯气不能用NaOH干燥,故D不选;
故选A.
点评 本题以气体干燥为载体考查元素化合物性质,明确物质性质及物质之间的反应是解本题关键,注意:浓硫酸还不能干燥硫化氢等还原性气体,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L F2所含原子数为0.1NA | |
| B. | 4.4gCO2中氧分子的个数为0.1NA | |
| C. | 78g Na2O2固体中Na+的个数目为NA | |
| D. | 2.3gNa完全燃烧后失去电子的个数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水分子的结构式是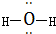 | |
| B. | NaCl的电子式为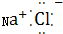 | |
| C. | 23Na37Cl中质子数和中子数之比是7:8 | |
| D. | 三氟化氮的电子式为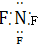 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.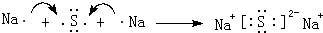 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
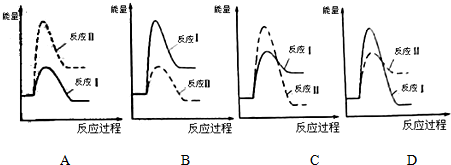
 Ba 2+(aq)+SO4 2-(aq)△H=+40KJ/mol.
Ba 2+(aq)+SO4 2-(aq)△H=+40KJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 单质 | A | B | C | D | E | F | G | H | I | J |
| 熔点(℃ | -150 | 550 | 160 | 210 | -50 | 370 | 450 | 300 | 260 | 250 |
| 与水反应 | ∨ | ∨ | ∨ | ∨ | ||||||
| 与酸反应 | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ||||
| 与氧气反应 | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ||
| 不发生化学反应 | ∨ | ∨ | ||||||||
| 相对于A元素的原子质量 | 1.0 | 8.0 | 15.6 | 17.1 | 23.8 | 31.8 | 20.0 | 29.6 | 3.9 | 18.0 |
| A | ||||||||||
| I | B | |||||||||
| J | ||||||||||
| H | ||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
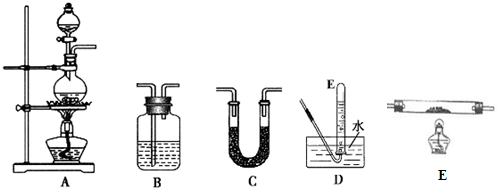
| 选用的仪器 | 加入的试剂 |
| A | 甲酸、浓硫酸 |
| D | -- |
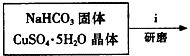
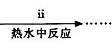
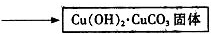
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+浓度减小 | B. | 溶剂质量减小 | C. | 溶液质量不变 | D. | Ca2+数目增多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com