
【题目】(1)除去Fe(OH)3胶体中混有的FeCl3的方法是_________________。
(2)在一定条件下,某固态化合物X受热分解的反应为:2X ![]() A↑+B↑+2C↑,测得反应后生成的混合气体的密度是同温同压下H2密度的12倍,则化合物X的摩尔质量为_______。
A↑+B↑+2C↑,测得反应后生成的混合气体的密度是同温同压下H2密度的12倍,则化合物X的摩尔质量为_______。
(3)将标准状况下的a L HCl气体溶于1 L水中,得到的盐酸密度为b g/cm3,则该盐酸的物质的量浓度为________________。
(4)现有某温度下饱和NaCl溶液V mL,密度为ρgcm-3,物质的量浓度为C molL-1则该温度下NaCl的溶解度为_________________(用V、ρ、C表示)。
(5)有A、B、C、D 四种可溶性盐,它们的阳离子是Ba2+、Ag+、Na+、Cu2+ 中的某一种,阴离子是NO3-、SO42-、Cl-、CO32- 的某一种。
①若把四种盐分别溶解于盛有蒸馏水的四只试管中,C盐的溶液呈蓝色。
②若向①的四只试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味气体逸出。
根据①②实验事实可推断它们的化学式为:
A、____________ C、______________ D、______________
【答案】渗析 48 g/mol 1000ab/(22400+36.5a)mol/L 5.85VC/(Vρ-0.0585VC)g BaCl2 CuSO4 Na2CO3
【解析】
(1)胶体粒子不能通过半透膜,而溶液中的粒子能通过半透膜。
(2)根据密度比等于相对分子质量之比和反应中的质量守恒进行分析。
(3)根据物质的量的基本公式计算。
(4)根据溶解度的定义进行计算。
(5)根据铜离子为蓝色进行分析,能反应的离子不能共存分析。
(1) 胶体粒子不能通过半透膜,而溶液中的粒子能通过半透膜,所以出去氢氧化铁胶体中的氯化铁可以用渗析的方法。
(2) 反应后生成的混合气体的密度是同温同压下H2密度的12倍,说明混合气体的相对分子质量为24,根据反应的质量守恒分析,假设2molX反应,则生成4mol气体,有关系式为2M(X)/4=24,解之得M(X)= 48 g/mol。
(3) 将标准状况下的a L HCl气体的物质的量为a/22.4,溶液的质量为(36.5a/22.4+1000)g ,溶液的体积为 (36.5a/22.4+1000)/1000b,该盐酸的物质的量浓度为a/22.4÷ (36.5a/22.4+1000)/ 1000b =1000ab/(22400+36.5a)mol/L。
(4)该溶液中氯化钠的物质的量为CV/1000mol,其质量为58.5CV/1000=0.0585CVg,溶液的质量为Vρg,假设溶解度为S,则有S/100=0.0585CV /( Vρ-0.0585VC) ,则S=5.85VC/(Vρ-0.0585VC)g。
(5)C盐的溶液显蓝色,说明为铜离子,四种试管中分别加入盐酸,B中有沉淀,说明为硝酸银。D中有无色无味的气体产生,说明含有为碳酸钠。则A为氯化钡,B为硝酸银,C为硫酸铜,D为碳酸钠。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】据国外资料报道,在独居石(一种共生矿,化学成分为Ce、La、Nd等的磷酸盐)中,查明有尚未命名的116、124、126号元素。判断其中116号应位于周期表中的( )
A.第六周期ⅣA族B.第七周期ⅥA族
C.第七周期Ⅷ族D.第八周期ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能,乙图是一种用惰性电极电解饱和食盐水的消毒液发生器。关于甲、乙的说法正确的是
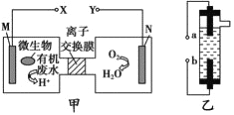
A. 装置乙中的b极要与装置甲的X极连接
B. 装置乙中a极的电极反应式为:2Cl- -2e-=Cl2↑
C. 当N极消耗5.6L(标准状况下)气体时,则有2NA个H+通过离子交换膜
D. 若有机废水中主要含有葡萄糖,则装置甲中M极发生的电极反应为: C6H12O6+6H2O-24e-=6CO2↑+24H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种元素位于周期表中同一周期,其最高价氧化物分别为酸性氧化物、碱性氧化物、两性氧化物,则这三种元素原子序数的大小顺序是( )
A.X>Y>Z
B.X>Z>Y
C.Y>X>Z
D.Y>Z>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究卤代烃与NaOH乙醇溶液反应的情况(已知乙醇可使酸性KMnO4溶液褪色),某化学课外小组的学生进行如下实验;
(1)甲同学用图1所示装置研究CH3CH2Br与NaOH的乙醇溶液的反应,充分反应后,试管D中的现象是_________________,试管C中水的作用是_______________,实验中________(填“能”或“不 能”)用Br2的四氯化碳溶液代替酸性高锰酸钾溶液。
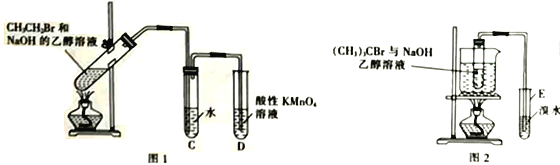
(2)乙同学用图2所示装置研究(CH3)3CBr与NaOH的乙醇溶液的反应。
①采用水浴加热的优点是_______________________________。
②发生反应后,试管E中的主要现象是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A元素原子的L层比B元素原子的L层少3个电子,B元素原子核外电子总数比A原子核外电子总数多5个电子,则A,B可形成的化合物为( )
A.A2B
B.AB2
C.B2A3
D.B3A2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 a L Al2(SO4)3 和(NH4)2SO4 的混合溶液分成两等份,向其中一份加入 b mol BaCl2,恰好使溶液中 的 SO42-完全沉淀;向另一份加入足量强碱并加热可得到 c mol NH3,则原溶液中 Al3+的浓度(mol/L)为
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用等质量铁与稀盐酸反应制备氢气时,欲使生成氢气的化学反应速率增大,下列措施可行的是( )
A.增加铁粒质量
B.换成同浓度的稀硫酸
C.改成98%的浓硫酸
D.加入纯硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是
A.NaHCO3与NaOH溶液反应:HCO3-+OH-===CO32-+H2O
B.氯气和水反应:Cl2+H2O ![]() 2H++Clˉ+ClOˉ
2H++Clˉ+ClOˉ
C.氯化铁溶液中加入足量的氨水:Fe3+ + 3NH3·H2O = Fe(OH)3 ↓+ 3NH4+
D.盛放碱性试剂的溶液不能用玻璃塞的原因:SiO2+2OH-===SiO32-+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com