
【题目】亚硝酸钠(有毒性,市场上很易与食盐混淆)是一种常见的工业用盐,广泛用于物质合成、金属表面处理等,它的用途、物理性质与NaCl极为相似。相关化学性质如图所示,下列说法不正确的是
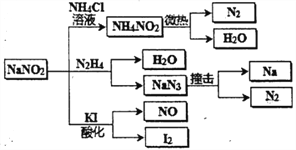
A. NaNO2稳定性大于NH4NO2
B. NaNO2与N2H4反应中,NaNO2是氧化剂
C. 可用KI-淀粉和食醋鉴别NaNO2 和NaCl
D. 分解NaN3盐每产生1molN2转移6mole-
科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。已知:p(Ba2+) = -lgc(Ba2+ ),p(SO42-)=-lgc(SO42-).下列说法正确的是( )
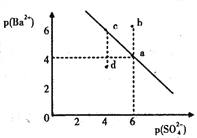
A. 该温度下,Ksp( BaS04) =1.0xl0-24
B. a 点的 Ksp(BaS04)小于 b 点的 Ksp(BaSO4)
C. d点表示的是该温度下BaS04的不饱和溶液
D. 加入BaCl2可以使溶液由c点变到a点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图实验装置制取乙酸乙酯。回答以下问题;
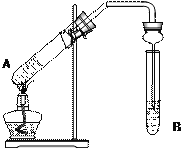
(1)在A试管中加入乙醇、乙酸和浓硫酸的顺序是_______________________________。
(2)写出A试管中发生反应的化学方程式___________________________________________
(3)B试管中所装液体应为___________,乙酸乙酯生成后,将在该溶液的______(填“上”或“下”)层,分离出该产品所需的主要仪器是_________________________________________
(4)该装置用球形干燥管代替长导管,并将干燥管的末端插入B中液面以下,在此处球形干燥管的作用有①_________________________________________________________
②_________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列的各种叙述中,正确的是( )
A.在任何条件下,纯水的pH=7B.在任何条件下,纯水都呈中性
C.在100℃时,纯水的pH>7D.在100℃时,纯水中c(H+)<10-7mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上曾经通过反应“3Fe + 4NaOH![]() Fe3O4+ 2H2↑+4Na↑” 生产金属钠。下列有关说法正确的是
Fe3O4+ 2H2↑+4Na↑” 生产金属钠。下列有关说法正确的是
A. 用磁铁可以将Fe与Fe3O4分离 B. 将生成的气体在空气中冷却可获得钠
C. 该反应条件下铁的氧化性比钠强 D. 每生成lmolH2,转移的电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. CaO与水反应过程中,有共价键的断裂和形成
B. H2O的热稳定性比H2S强,是由于H2O的分子间作用力较大
C. KCl、HCl、KOH的水溶液都能导电,所以它们都属于离子化合物
D. 葡萄糖、二氧化碳和足球烯(C60)都是共价化合物,它们的晶体都属于分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式己配平): Cu+2H2SO4(浓)![]() CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成,则A应该属于______(填序号)
a.电解质 b.非电解质 c.硫化物 d.酸性氧化物 e.碱性氧化物
(2)A物质可以使酸性KMnO4溶液褪色,此反应中______(填写化学式,下同)失去电子,还原产物是______。
(3)一定量的铜片与100mL18mol/L的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的质量为______g,发生还原反应的硫酸的物质的量为___________mol。
(4)将反应后所得到的溶液与足量Ba(OH)2溶液充分反应。请写出此过程发生的反应的离子方程式:______、_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数值,下列说法正确的是
A. 室温下,21.0g 乙烯与丙烯的混合气体中含有的碳原子数为1.5NA
B. 常温常压下,0.1molC8H18所含有的共价键数目为2.0 NA
C. 0.1mol乙醇与氧气完全反应生成二氧化碳时转移电子数为0.1NA
D. 标准状况下,2.24L乙酸乙酯中所含氧原子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com