
【题目】某非金属单质A经下图所示的过程转化为含氧酸D,
![]()
已知D为强酸,请回答下列问题:
(1)若A常温下为淡黄色固体,B是有刺激性气味的无色气体。
①氯水和B皆可作漂白剂。若同时使用于漂白一种物质时,其漂白效果是________(填“增强”“减弱”“不变” ),用化学方程式解释上述原因 ;
②D的浓溶液与铜发生反应的化学方程式: 。
(2)若A在常温下为气体,C是红棕色气体。
①A转化为B的化学方程式是:______________________________________,
② D的稀溶液在常温下可与铜反应并生成B气体,请写出该反应的离子方程式: 。
【答案】(1)①减弱 SO2+Cl2+2H2O=2HCl+H2SO4 ②Cu+2H2SO4 (浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(2)①N2+O2![]() 2NO ② 3Cu + 8 H++2NO3-=3Cu2++ 2 NO↑+ 4 H2O
2NO ② 3Cu + 8 H++2NO3-=3Cu2++ 2 NO↑+ 4 H2O
【解析】
试题分析:(1)若A常温下为淡黄色固体,B是有刺激性气味的无色气体,说明A是S,B是二氧化硫,C是三氧化硫,D是硫酸;
①氯水和B皆可作漂白剂,若同时使用于漂白一种物质时,会发生反应SO2+Cl2+2H2O=2HCl+H2SO4,其漂白效果将减弱;
②D的浓溶液与铜发生反应的化学方程式为Cu+2H2SO4 (浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(2)若A在常温下为气体,C是红棕色气体,则A是氮气,B是一氧化氮,C是二氧化氮,D是硝酸;
①A转化为B的化学方程式是:N2+O2![]() 2NO;
2NO;
② D的稀溶液在常温下与铜反应并生成B气体,离子方程为3Cu + 8 H++2NO3-=3Cu2++ 2 NO↑+ 4 H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某元素X的气态氢化物化学式为H2X,下面的叙述不正确的是
A.该元素的原子最外层上有6个电子
B.该元素最高价氧化物的化学式为XO2
C.该元素一定是非金属元素
D.该元素最高价氧化物对应水化物的化学式为H2XO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“保护环境,就是保护人类自己”。下列环境问题与其产生的主要原因不相符有几个?( )
①“光化学烟雾”主要是由NOx等引起的
②“白色污染”主要是由聚乙烯塑料等引起的
③“温室效应”主要是由空气中CO2浓度增大引起的
④“臭氧空洞”主要是大量使用氟氯代烃等引起的
⑤“赤潮”主要是由水体中P、N等元素过量引起的
⑥“酸雨”主要是由空气中SO2、NOx、CO2浓度增大引起的
⑦“PM2.5”主要由化石燃料的燃烧(如机动车尾气、燃煤)等引起的
A.0个B.1个C.2个D.3个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:NH2COO-+2H2O![]() HCO3-+NH3˙H2O。现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是
HCO3-+NH3˙H2O。现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是

A.无法判断T1和T2的大小关系
B.T1℃时,第6min反应物转化率为6.25%
C.T2℃时,0~6minν(NH2COO-)=0.3molL-1min-1
D.往平衡体系加水稀释,平衡右移,溶液中各种离子浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某化学小组为测定一定质量的某镁铝混合物中镁、铝的质量分数,设计了如下实验方案:
取ag镁铝混合物![]() 测定剩余固体的质量为bg当溶液B为NOH溶液时,铝的质量分数为___________。
测定剩余固体的质量为bg当溶液B为NOH溶液时,铝的质量分数为___________。
(2)现有甲、乙两瓶无色溶液,已知它们可能是AlCl3溶液和NaOH溶液。现做如下实验:
①取440mL甲溶液与120mL乙溶液反应,产生1.56g沉淀。
②取120mL甲溶液与440mL乙溶液反应,产生1.56g沉淀。
③取120mL甲溶液与400mL乙溶液反应,产生3.12g沉淀。
通过必要的计算和推理判定:甲溶液为____________溶液,理由是:___________________________________________________________________________
甲溶液的物质的量浓度是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:(无特殊说明均填元素符号、化学式等化学用语)
主族 | IA | ⅡA | IIIA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ⑥ | |||
3 | ⑦ | ⑧ | ⑨ | |||||
4 | ⑩ |
(1)在这些元素中,化学性质最不活泼的是 ,元素原子半径最小的是 ,被称为“国防金属”的是 ,可作为半导体材料的是 ,单质氧化性最强的元素是 。
(2)元素②的一种同位素(含8个中子)可测定文物年代,这种同位素的符号是 。
(3)在上述元素的最高价氧化物对应水化物中,碱性最强的化合物的化学式是 。酸性最强的化合物的化学式是 。
(4)写出③的气态氢化物与其最高价氧化物对应水化物反应的方程式 。
(5)元素④的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数小于36的X、Y、Z、W、R五种元素,原子序数依次增大。五种元素中,仅R为金属元素,其原子序数为27。X价电子排布式为nsnnpn,元素Z基态原子s电子总数与p电子总数相等,W与其它四种元素能层数不同,且未成对电子数目为1个。
根据判断出的元素回答下列问题:

(1)基态R原子核外电子排布式为 。
(2)1mol配合物[R(XY)6]4-中含有σ键的数目为 。
(3)XZW2是一种高毒类物质,结构与甲醛相似,X原子杂化方式为 ,其沸点高于甲醛的主要原因是 。
(4)YW3为黄色、油状、具有刺激性气味的液体,该分子的立体构型为 (用文字描述)。
(5)R与某元素A构成的晶体的晶胞结构如下图所示,则R的配位数是 ,A的配位数是 。
(6)在答卷的图中画出与顶点m配位的所有A原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别写出满足下列叙述中有关物质的结构简式或化学方程式:
(1)能与金属钠反应,但不能与氢氧化钠反应的芳香族化合物C7H8O是 。
(2)分子式为C3H7Br的卤代烃经消去反应后得到的有机物是 ;
(3)含C、H、O三种元素的有机物,完全燃烧时消耗的氧气和生成的CO2、H2O之间物质的量之比为1:1:1,则此类有机物中最简单的一种是 。
(4)苯酚与饱和溴水的反应方程式为 ,该反应用于苯酚的 和 。
(5)TNT(2,4,6-三硝基甲苯)是一种烈性炸药,广泛用于国防、开矿、筑路等,写出制备TNT的方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 W、X、Y、Z 在元素周期表中的位置如右图所示。其中 Z 的单质是一种重要半导体材料,广泛应用于电子工业的各个领域。
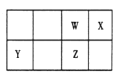
(1)W 在元素周期表中的位置是____________。
(2)W、X、氢元素形成的三原子分子的电子式____________。
(3)下列选项中,能证明元素非金属性X强于W的是____________。
A.相对原子质量:X>W | B.最低化合价:X>W |
C.最简单氢化物的稳定性:X>W | D.最高价氧化物的水化物酸性:X>W |
(4)元素周期表中与 Z 同周期的某金属元素形成的单质 A,可发生如下图所示的转化:
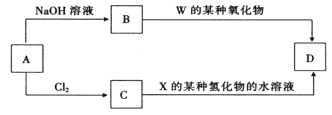
其中化合物D是一种白色沉淀,则 B 中溶质的化学式为____________;
B与 C也可直接转化生成 D 写出对应的离子方程式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com